Questões de Concurso
Comentadas sobre interações atômicas: ligações iônicas, ligações covalentes e ligações metálicas. ligas metálicas. em química
Foram encontradas 96 questões
I - O calor liberado na hidrogenação do benzeno é menor que o liberado na hidrogenação de um trieno não aromático.
II - O benzeno sofre reações de adição de bromo (Br2 ) nas suas duplas ligações.
III - Segundo a Teoria do Orbital Molecular (TOM), o benzeno possui três orbitais moleculares π ligantes preenchidos com elétrons, além de apenas um orbital molecular antiligante.
IV - Por possuir ligações duplas e simples, há ligações carbono-carbono com diferentes comprimentos no benzeno.
Está correto APENAS, o que se afirma em
HCℓ, KCℓ, MgCℓ2, CH2C ℓ2 e CC ℓ4.
Desses compostos, aqueles que apresentam ligação iônica são
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
A estrutura de Lewis para o íon tetrafluoroborato (BF4 − ) é a mostrada a seguir.
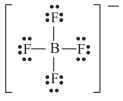
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O físico-químico Gilbert Newton Lewis propôs a regra do
octeto.
Acerca de ligações químicas e estruturas moleculares, julgue o item seguinte.
O físico-químico Gilbert Newton Lewis explicou o modelo
das ligações químicas.
Via de regra, os aços mais dúcteis, largamente utilizados em elementos estruturais e tubulações, são aços:
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

O fato de o NaCl fundir-se a 801 °C e o MgO fundir-se a 2.852 °C é uma evidência de que os sólidos iônicos são unidos por interações entre cátions e ânions, isto é, ligações iônicas.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

Os sólidos iônicos são cristalinos, e os sólidos moleculares são amorfos.
O gráfico seguinte mostra um diagrama de fases genérico de uma substância pura.

As moléculas se organizam por meio de ligações covalentes entre si para formar os sólidos moleculares.
Uma das principais vantagens da teoria de ligação de valência é a possibilidade de explicar, satisfatoriamente, fenômenos associados a estados de excitação e de prever os espectros de absorção e emissão de energia eletrônica das moléculas.
Nos compostos formados por cátions e ânions muito polarizáveis, o caráter da ligação química é fortemente covalente.
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
De acordo com a teoria de ligação de valência, a molécula de água é constituída por quatro orbitais híbridos do tipo sp3 arranjados de forma tetraédrica em torno do oxigênio, de maneira que dois orbitais participam das ligações simples O–H e outros dois acomodam os pares de elétrons não ligantes.
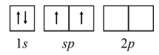
De acordo com a teoria de ligação de valência, o diagrama de orbitais para o átomo de Be, para formar orbitais híbridos no BeF2, está corretamente representado na figura a seguir.
O comprimento da ligação entre o hidrogênio e o átomo de halogênio é maior no HI que no HF.
Nas ligações covalentes entre átomos diferentes, os pares de elétrons são compartilhados igualmente.
Cátions e ânions estão mais fortemente ligados no NaCl que no KCl.