Questões de Concurso Comentadas sobre química
Foram encontradas 7.276 questões
(1) Ácido de Lewis ( ) NH3
(2) Base de Arrhenius ( ) CH3COOH
(3) Base fraca de Bronsted-Lowry ( ) KNO3
(4) Ácido forte de Bronsted-Lowry ( ) HCl
(5) Componente ácido de tampão ( ) NH4Cl
(6) Componente salino de tampão ácido ( ) BF3
(7) Sal ácido ( ) CH3COONa
(8) Sal neutro ( ) KOH
A sequência numérica correta de preenchimento dos parênteses da coluna da direita, de cima para baixo, é
H2S LiOH CuBr2 NaNO3 KF SO3 Na2O
Pode-se afirmar que as soluções apresentam, da esquerda para a direita, valores de pH a 25 ºC, conforme listados a seguir:
I - A temperatura de equilíbrio será 50 ºC.
II - A água fria sofre aumento de energia interna e de entropia.
III - A água fria sofre aumento de entalpia e diminuição de entropia.
IV - A água quente sofre diminuição de energia interna e aumento de entropia.
Quais estão corretas?
Líquido Densidade (g/mL) benzeno 0,884 clorofórmio 1,477 éter dietílico 0,710 xileno 0,872
A água salgada do Mar Morto possui densidade igual a 1,240 kg/L, enquanto a da água pura pode ser considerada unitária.
A situação abaixo foi encontrada durante uma extração.
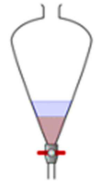
A camada superior e a camada inferior podem ser, respectivamente,
I - Fórmula química do solvente e concentração da solução de limpeza.
II - Concentração comum da solução e concentração molar do soluto.
III - Peso dos metais pesados na solução final e concentração da solução salina.
Quais correspondem aos principais cálculos que devem ser utilizados no preparo de soluções?
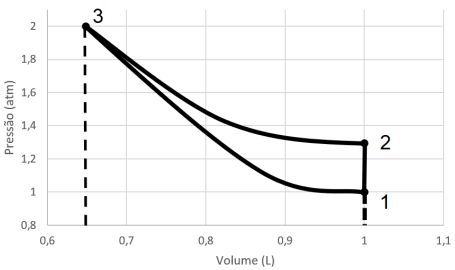
I. A variação de entropia ao longo do ciclo é nula. II. A variação de trabalho ao longo do ciclo é nula. III. A variação de energia interna ao longo do ciclo é nula.
Assinale

Pesos moleculares: I=127 g/mol; K= 39 g/mol; O= 16 g/mol; C=12 g/mol.
Reações de neutralização são reações entre um ácido e uma
base que produzem sal e água, de acordo com os conceitos de
Arrhenius. O sal inorgânico formado é então um produto iônico
dessa reação que ao ter contato com a água é dissolvido liberando
no mínimo um cátion diferente de H+ e no mínimo um ânion
diferente de OH-. Considerando a dissolução de um sal em uma
solução aquosa neutra, assinale a alternativa correta.
As figuras a seguir ilustram quatro curvas de titulação volumétrica de neutralização (A, B, C e D), envolvendo ácidos e bases de concentrações iguais.
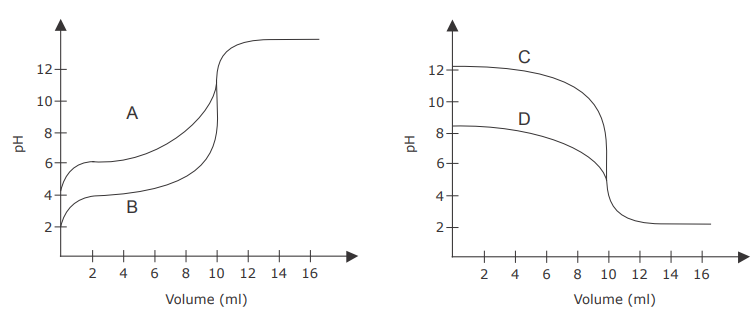
Em relação às curvas de titulação da figura, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) A curva "A" representa a titulação de um ácido fraco com uma base forte.
( ) A curva "B" representa a titulação de um ácido muito fraco com uma base forte.
( ) A curva "C" representa a titulação de uma base fraca com um ácido forte.
( ) A curva "D" representa a titulação de um ácido fraco com uma base forte.
A sequência correta é
Para a determinação colorimétrica de um composto "X" na faixa de concentração de 1 a 8 mg/L, um analista realizou a medida de absorvância para 4 padrões em um colorímetro de bancada. A curva de calibração preparada pelo analista pode ser visualizada na figura.
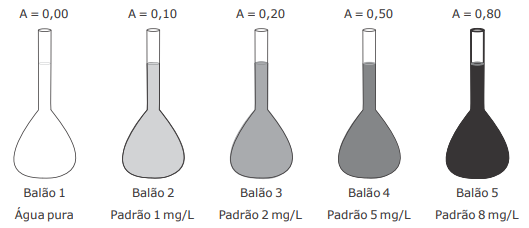
Sabendo que a análise do composto "X" deve apresentar absorvância no intervalo entre 0,10 e 0,80 e que o
rótulo da amostra contendo o composto "X" indica uma concentração de 2000 mg/L, considere as afirmativas
a seguir.
I - A amostra precisa ser diluída 100 vezes para que possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
II - 1 mL da amostra deve ser pipetado em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
III - 5 mL da amostra devem ser pipetados em um balão volumétrico de 500 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
IV - 1 mL da amostra deve ser pipetado em um balão volumétrico de 250 mL e o volume aferido com água desionizada, para que essa amostra possa ser medida pelo método colorimétrico proposto no intervalo de concentração e absorvâncias mostrado na figura.
Está(ão) correta(s)
SOLUÇÃO 1 - 10 mL da solução estoque (2,010 mol/L) foi pipetado e transferido para um balão volumétrico de 100 mL, onde o volume foi completado com água desionizada.
SOLUÇÃO 2 - 5 mL da SOLUÇÃO 1 foi pipetado e transferido para um balão volumétrico de 50 mL, onde o volume foi completado com água desionizada.
As concentrações finais da SOLUÇÃO 1 e SOLUÇÃO 2 são, respectivamente,
