Questões de Concurso Sobre química
Foram encontradas 13.364 questões

Internet:<www.tabelaperiodica.org>
Quanto à espectroscopia de absorção molecular no infravermelho, julgue o item.
As bandas no espectro de absorção no infravermelho
correspondem aos modos vibracionais das ligações
químicas.

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
O termo “deslocamento hipsocrômico” é usado para
descrever a mudança da banda de absorção para
regiões do espectro onde o comprimento de onda
é maior

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
O termo “deslocamento batocrômico” é utilizado
para descrever a mudança da banda de absorção para
regiões do espectro onde a energia é menor.

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
Na absorção molecular, os alcanos apresentam transições do tipo σ → σ , enquanto os compostos carbonílicos apresentam transições do tipo σ → π* .

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
À medida que o número de moléculas capazes de absorver luz de um determinado comprimento de onda aumenta, a extensão dessa absorção diminui, de acordo com a Lei de Lambert‑Beer expressa pela equação a seguir.
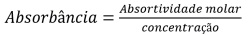

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
Um efeito hipercrômico refere‑se ao aumento da
intensidade da banda.

Internet:<www.tabelaperiodica.org>
Considerando as estruturas e as geometrias moleculares, julgue o item.
Uma molécula com geometria quadrado planar
apresenta quatro ligantes, dois pares de elétrons
isolados e um arranjo eletrônico octaédrico.

Internet:<www.tabelaperiodica.org>
Considerando as estruturas e as geometrias moleculares, julgue o item.
Uma molécula com geometria do tipo gangorra
apresenta quatro ligantes e um par de elétrons
isolado.

Internet:<www.tabelaperiodica.org>
Considerando as estruturas e as geometrias moleculares, julgue o item.
A molécula BCl3
apresenta geometria trigonal plana.

Internet:<www.tabelaperiodica.org>
Considerando as estruturas e as geometrias moleculares, julgue o item.
A amônia é uma molécula covalente que contém
hibridização sp2
e um par de elétrons isolado.

Internet:<www.tabelaperiodica.org>
Considerando as estruturas e as geometrias moleculares, julgue o item.
A sobreposição dos orbitais hibridizados C‑C no etano
é do tipo sp3
‑sp3
.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
Na teoria do orbital molecular, a ordem de ligação (O.L) é calculada por meio da equação a seguir.
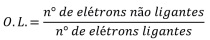

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
Na teoria do orbital molecular, o diagrama de níveis
de energia indica que a ligação entre dois átomos de
hélio resulta em uma ordem de ligação de zero.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
No ácido sulfúrico, existem somente ligações
sigmas (σ).

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
Na ligação covalente, a carga formal corresponde ao
número de oxidação dos átomos.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
A ligação sigma (σ) é formada pela sobreposição
frontal dos orbitais atômicos.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
No gráfico de potencial de Morse, a energia
da molécula atinge um mínimo quando há um
balanceamento entre as atrações e as repulsões.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
A energia de rede independe do raio iônico.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
Todos os compostos iônicos são condutores de
eletricidade, independentemente do estado de
agregação.

Internet:<www.tabelaperiodica.org>
Quanto às ligações químicas, julgue o item.
Compostos iônicos, geralmente, possuem pontos de
fusão e ebulição baixos, pois os íons são unidos por
forças eletrostáticas, e não por ligação covalente.