Questões de Concurso Sobre química
Foram encontradas 13.364 questões
I. Ar.
II. Sangue.
III. Granito.
IV. Madeira.
V. Gasolina.
VI. Soro fisiológico.
São exemplos de misturas heterogêneas o que se afirma apenas em
Observe a figura abaixo.
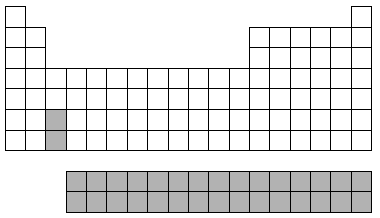
O modelo construído e proposto da figura agrupa os elementos químicos conhecidos e suas
propriedades e está organizado em ordem crescente de
I. A mistura de 5 g de soluto em 250 mL de água destilada resultará em uma solução 2% m/V.
II. O hidróxido de magnésio, vendido em farmácias para azia, é considerado como uma solução verdadeira e homogênea.
III. O ácido clorídrico é considerado um padrão primário, implicando que sua solução não requer análises para a determinação da concentração real.
Está correto o que se afirma apenas em
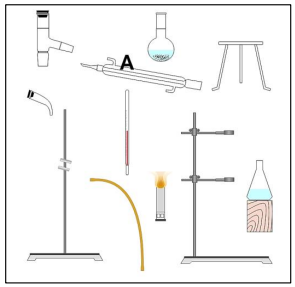
Sobre os processos de separação e, ainda, considerando disposto na imagem anterior, assinale a afirmativa correta.
C6H14 + O2 → CO2 + H2O
A massa de oxigênio necessária para reagir completamente com 2 mols de hexano será de, aproximadamente:
• Massa inicial da amostra de efluente: 50 g • Massa do papel de filtro utilizado: 0,5 g • Massa final do precipitado seco e papel de filtro: 3,8 g • Massa do reagente que precipitou: 0,8 g • Volume da amostra de efluente analisado: 0,5 L
Com base nessas informações, a concentração do contaminante no efluente em gramas por litro (g/L) é de, aproximadamente:
PbSO4 (s) ⇌ Pb2+(aq) + SO2–4 (aq)
A constante de equilíbrio (Kps) para essa reação é conhecida e equivale a 1,0 × 10−8 . Com base no equilíbrio iônico de solubilidade, a concentração máxima de íons de chumbo (Pb²⁺) na água tratada antes que o PbSO₄ comece a precipitar será de:
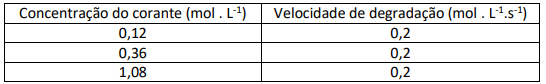
Os dados experimentais apresentados na tabela sugerem uma lei cinética de degradação de ordem:
( ) Geralmente, a técnica espectroscópica prescinde do uso de branco como referência antes de todas as medidas.
( ) Transições eletrônicas que implicam mudança de spin do elétron são permitidas e, frequentemente, originam bandas com elevada intensidade de absorção.
( ) A intensidade e o perfil das bandas de absorção do composto são independentes do solvente utilizado.
A sequência está correta em
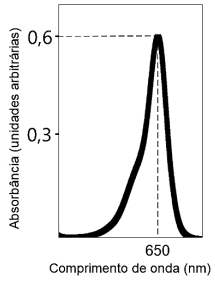
Considerando o espectro coletado e um coeficiente de absortividade molar de 40.000 L/(mol.cm) para o analito, a concentração da substância em µmol/L (micromol/L) determinada pela Lei de Lambert-Beer será de, aproximadamente:
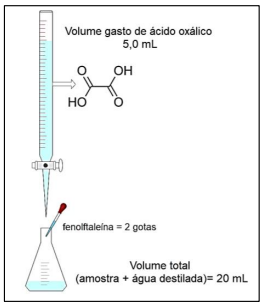
Considerando as informações fornecidas e a imagem, a concentração real da solução preparada de NaOH será de:
Assinale a alternativa que apresenta a quantidade de orceína a ser adicionada no preparo do corante.
Sobre o preparo dessa solução de HCl, assinale V (verdadeiro) ou F (falso) em cada afirmativa a seguir.
( ) Para o preparo da solução, serão necessários 84ml de HCl e 1000 ml de água destilada.
( ) Para evitar acidentes no laboratório, deve-se adicionar primeiramente a água destilada e posteriormente o HCl.
( ) Para uma medição precisa do volume da solução, deve-se utilizar um becker de vidro graduado, pois essa vidraria é mais precisa em relação aos balões volumétricos e às provetas.
A sequência correta é
Sabendo que as massas moleculares aproximadas do tris (ou tris-hidroximetil-aminometano) e do EDTA (ácido etilenodiaminotetra-acético) são 121 u e 292 u, respectivamente, para preparar 500 mL de TE 10 X é necessário pesar
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Em um modelo simplificado para uma bateria de íon-lítio
com anodo de grafite e catodo com substrato de cobalto
dopado com lítio, para descrever adequadamente o processo,
pode-se usar uma equação global do tipo
LiC6 + CoO2 ⮂ C6 + LiCoO2, cuja reação direta diz respeito
à descarga e a inversa, à carga.
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Para o mesmo peso, uma bateria de níquel-cádmio é capaz de
fornecer maior quantidade de watts x horas que uma bateria
de íon-lítio, mas em um intervalo de tempo maior.
Baterias de íon-lítio são um dos tipos de bateria recarregável mais amplamente utilizados na atualidade. A base de funcionamento desses dispositivos é a transferência de íons de lítio entre um catodo e um anodo. Em comparação com outras tecnologias, como níquel-cádmio ou níquel-hidreto, as baterias de íon-lítio apresentam maior densidade de energia, menor efeito de memória e menor perda de carga quando em uso.
A respeito das baterias de íon-lítio, julgue o item que se segue.
Às reações químicas que ocorrem nesse tipo de bateria
podem ser atribuídas constantes de equilíbrio.