Questões de Concurso Sobre química
Foram encontradas 13.364 questões
4Fe(s) + 3O2(g) + 2H2O(l) → 2Fe2O3.H2O(s)
Uma das maneiras de evitar esse fenômeno é

O volume do ácido sulfúrico concentrado necessário para preparar a solução solicitada pelo professor foi de, aproximadamente,
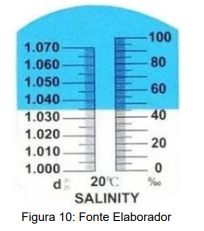
Conforme a leitura realizada, é correto afirmar que a concentração de sais dissolvidos na água é de, aproximadamente,
C3H6O3 + NaOH → Na(C3H5O3) + H2O
KMnO4 + H2SO4 + CH3CH2OH → K2SO4 + MnSO4 + CH3CHO + H2O + calor
A soma dos coeficientes, após o balanceamento, é de
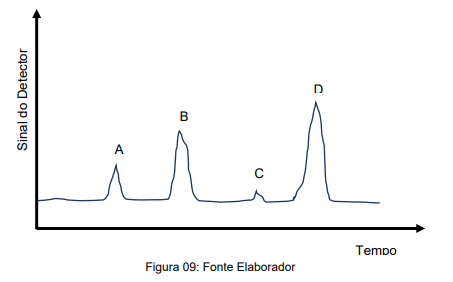
Com base nesse cromatograma, é correto afirmar que
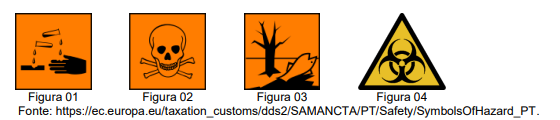
Cada símbolo, chamado pictograma, possui um significado universal. Os símbolos acima representam, respectivamente
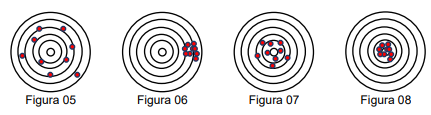
De acordo com o observado nas figuras, é correto afirmar que elas representam, respectivamente,
Para determinar o teor de matéria seca e o teor de umidade de determinada amostra de ração animal, usando o método gravimétrico, pesaram em cadinhos de porcelana, isentos de umidade, cujo peso havia sido determinado previamente, em torno de 2,0 g das amostras em balança analítica. Os cadinhos com as amostras foram levados à estufa, préaquecida a 105° C até peso constante (4 a 6 horas) ou por mínimo de 6 h. Após esse período, colocaram-se as amostras no dessecador até temperatura ambiente para a pesagem final. Fez-se o procedimento em triplicata e trabalhou-se com a média dos resultados. Os resultados seguintes estão em valores aproximados para facilitar os cálculos. Os valores dos pesos estão em gramas.
A partir dessas informações, o valor aproximado para o teor de umidade (em %) da amostra analisada é de
Duas amostras de compostos carbonilados distintos W e Z foram submetidos ao seguinte teste:
Em um tubo de ensaio foram colocados 2 mL de uma solução de AgNO3 5% e adicionou-se 1 gota de uma solução diluída de NaOH 10%. Juntou-se gota a gota uma solução de NH4OH 2%, agitando até o desaparecimento do precipitado de óxido de prata e formação do complexo diaminoprata (reativo de Tollens).
Num outro tubo identificado como W: colocou-se 1 mL do reativo de Tollens (recentemente preparado) e duas gotas de W. Repetiu-se o procedimento para outro tubo identificado como Z, adicionando duas gotas de Z a 1mL do reativo de Tollens. Sem agitar, observou-se a formação de espelho de prata no tubo Z.
A partir desse resultado, o composto Z pode ser
n-hexílico, t-butílico, n-butílico, n-pentílico, s-butílico, aquele com fórmula molecular C4H10O que apresenta o menor valor para a temperatura de ebulição, em graus Celsius, é o álcool