Questões de Concurso Sobre química
Foram encontradas 14.919 questões
Reações químicas com óxidos são processos químicos que ocorrem quando substâncias desse grupo de substâncias inorgânicas reagem com água (H2O), base ligada a um metal ou amônio e ácido ligado a um ânion qualquer.Os óxidos são substâncias bastante reativas, o que faz deles formadores de diversas outras substâncias.De acordo com os diferentes tipos, os óxidos podem ser:
I. Óxidos ácidos.
II. Óxidos básicos.
III. Óxidos neutros.
IV. Óxidos anfóteros.
V. Óxidos duplos, mistos ou salinos.
Estão CORRETAS:
A poluição do ar pode ser definida como a presença de substâncias provenientes de atividades humanas ou da própria natureza que podem colocar em risco a qualidade de vida dos seres vivos. O ar poluído pode causar sérios problemas ao homem e a outros seres, portanto, ele é impróprio e nocivo.
Sobre a poluição do ar é correto afirmar que, EXCETO:
Observe a figura do equipamento laboratorial, a seguir

Esse equipamento é indicado para:
De modo geral, na técnica de absorção atômica, a solução que contém o analito de interesse é inserida no equipamento sob a forma líquida, e é convertida em um fino aerossol antes de atingir o atomizador.
Assinale a alternativa que apresenta o modo de
atomização mais adequado à afirmativa descrita
anteriormente.
Muitos íons metálicos formam complexos estáveis, solúveis em água, com muitas aminas terciárias. A formação desses complexos serve como base nas titulações complexométricas de íons metálicos.
Sobre as titulações complexométricas, assinale a alternativa INCORRETA.
A produção comercial do ácido nítrico envolve as seguintes reações químicas:
I. 4NH3(g) + 5O2(g ) → 4NO(g) + 6H2O(g)
II. 2NO(g) + O2(g) → 2NO2(g)
III. 3NO2(g) + H2O(L) → 2HNO3(aq) + NO(g)
É correto afirmar que são reações de oxirredução as descritas em:
Em todas as grandes áreas da Química e, em especial, na Química Analítica, é necessário que o profissional saiba distinguir e utilizar convenientemente cada equipamento volumétrico de modo a reduzir ao mínimo os erros nas análises.
Sobre os instrumentos volumétricos, assinale com V as afirmativas verdadeiras e com F as falsas.
( ) As pipetas e buretas são instrumentos construídos e calibrados para contenção de volumes.
( ) A precisão alcançável com uma pipeta é substancialmente maior que a precisão de uma bureta.
( ) Os frascos volumétricos são utilizados para a preparação de soluções-padrão e para a diluição de amostras, a volumes fixos, antes da tomada de alíquotas com uma pipeta.
( ) As buretas são instrumentos volumétricos de transferência de líquidos utilizadas para escoar volumes variáveis e empregadas geralmente em titulações.
Assinale a sequência CORRETA.
A curva para a titulação de um ácido fraco por uma base forte é muito similar no formato àquela para a titulação de um ácido forte por uma base forte. Quando ácidos fracos contêm mais de um átomo de hidrogênio ionizável, como no ácido fosfórico (H3PO3 ), a reação com OH- ocorre em uma série de etapas.
Considere o gráfico a seguir, que representa a curva de titulação para a reação de 50 mL de 0,1 mol/L de H3PO3 com 0,1 mol/L de NaOH.
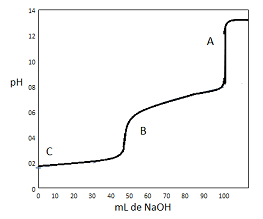
Segundo a curva de titulação, as espécies químicas A, B
e C são, respectivamente:
Nos anos de 1950, tanto os Estados Unidos quanto a antiga União Soviética tinham programas para usar o decaborano (B10H14) como combustível de foguete. Esse composto reage violentamente com oxigênio, de acordo com a equação química a seguir.
B10H14 + 11 O2 → 5 B2O3 + 7 H2O
Na tentativa de simular a eficiência máxima do foguete, considere que um engenheiro elaborou um projeto que consumiu o decaborano (B10H14) com 80% de pureza.
Sabendo que 10 mil kg do decaborano foram colocados para reagir com oxigênio, aproximadamente quantos mols de moléculas do B2O3 foram produzidos na reação?
A espectroscopia de absorção atômica em chama (EAA) é correntemente o método atômico mais empregado em razão de sua simplicidade, efetividade e custo relativamente baixo.
Numere a COLUNA II de acordo com a COLUNA I relacionando os instrumentos empregados na técnica de absorção atômica à sua aplicabilidade.
COLUNA I
1. Fonte
2. Célula de absorção
3. Monocromador
4. Detector
5. Registrador
COLUNA II
( ) Mede a intensidade de luz e a transforma em sinal elétrico.
( ) Mostra a leitura depois de o sinal ser processado.
( ) Emite o espectro do elemento de interesse.
( ) Seleciona o comprimento de onda a ser utilizado.
( ) Local onde os átomos da amostra são produzidos.
Assinale a sequência CORRETA.
Sobre alguns compostos moleculares, considere que um estudante faz as seguintes classificações:
I. Composto CO2 (forma geométrica linear e molécula apolar).
II. Composto H2S (forma geométrica angular e molécula polar).
III. Composto CH2O (forma geométrica tetraédrica e molécula polar).
Estão corretas as classificações:
Considere, hipoteticamente, que, em um estudo cinético de formação do composto AB, a reação ocorre nas seguintes condições experimentais: uma reação de primeira ordem em relação a A e de segunda ordem em relação a B.
Nessas condições, a velocidade da reação química aumenta quantas vezes se as concentrações das espécies A e B forem duplicadas?
Considere que no preparo de uma solução de HCl 0,1 mol/L um técnico utiliza 4,5 mL da solução de estoque do reagente concentrado. A solução de estoque tem as seguintes especificações:

Nessas condições, e para garantir uma concentração
mais próxima possível daquela que o técnico pretende,
é correto afirmar que o balão volumétrico utilizado para
o preparo dessa solução é de:
A segurança dos profissionais da área de Química nos laboratórios é extremamente importante para o bom desempenho das atividades experimentais. Com a finalidade de reduzir a frequência e a gravidade de acidentes nos laboratórios, torna-se absolutamente imprescindível que, durante os trabalhos realizados, se observe uma série de normas de segurança. A armazenagem dos reagentes, por exemplo, deve ser com seus rótulos originais e, quando isto não for possível, a etiqueta deve conter, no mínimo, o nome químico do reagente, sua composição e os principais riscos.
Sobre os possíveis riscos à saúde decorrentes da exposição a alguns produtos químicos, assinale a afirmativa INCORRETA.
Na oxidação de álcoois, o carbono que sofre oxidação é sempre aquele ligado à hidroxila. Dependendo do tipo de álcool que reage, a oxidação dos álcoois pode originar aldeídos, cetonas, ácidos carboxílicos, gás carbônico e água.
Enumere a COLUNA II de acordo com a COLUNA I relacionando o composto com a(s) substância(s) produzidas na oxidação completa do álcool.
COLUNA I
1. Etanol
2. Metanol
3. Propano-2-ol
COLUNA II
( ) Cetona
( ) Gás carbônico e água
( ) Ácido carboxílico
Assinale a sequência CORRETA.
A lei de absorção, também conhecida como lei de Beer-Lambert ou somente lei de Beer, diz quantitativamente como a grandeza da atenuação depende da concentração das moléculas absorventes e da extensão do caminho sobre o qual ocorre a absorção.
Considere, hipoteticamente, que uma solução 0,10 mol/L de permanganato de potássio (KMnO4 ) apresenta uma absorbância igual a 0,340, quando medida em uma célula de 2,0 cm no comprimento de 525 nm.
Nessas condições, é correto afirmar que a absortividade molar do KMnO4 é igual a:
A concentração do hidróxido de sódio (NaOH) pode ser determinada via titulação por uma solução-padrão de ácido clorídrico (HCl). Considere que nesse processo de titulação foram consumidos 25 mL de HCl 0,1 mol/L.
Sabendo que o volume da base é de 50 mL, é correto afirmar que a concentração NaOH em gramas por litro é igual a:
Relacione a COLUNA I com a COLUNA II, associando as substâncias a serem quantificadas aos métodos de análise adequados para quantificação de cada substância.
COLUNA I
1. Espectroscopia de absorção atômica em forno de grafite
2. Espectroscopia de absorção atômica com geração de hidreto
3. Espectrofotometria no ultravioleta
4. Fluorimetria
COLUNA II
( ) Chumbo em água de abastecimento humano
( ) Glicerol em suco de fruta
( ) Mercúrio em peixe de água doce
( ) Quinino em água tônica
( ) Selênio em suplemento mineral
( ) Tiamina em medicamento parenteral
Assinale a sequência CORRETA.