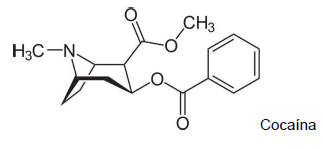
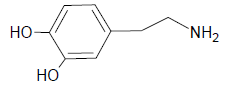
Questões de Concurso Sobre química
Foram encontradas 13.542 questões
Assinale a alternativa que apresenta as vidrarias
de laboratório que permitem precisar o volume das
substâncias com maior exatidão.
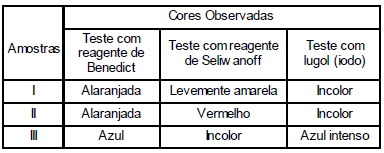
As atividades práticas no ensino de Ciências são uma ferramenta de grande importância para auxiliar no processo de aprendizagem dos alunos, e o interesse pela ciência aumenta quando são envolvidos itens do cotidiano. Um grupo de alunos levou algumas amostras ao laboratório de química e realizou três testes de identificação de carboidratos. Os resultados são apresentados no quadro abaixo:
Caixas de merenda de escolas estaduais dividem espaço com tambores de empresas de produtos químicos no galpão de uma empresa de logística em Guarulhos, na Grande São Paulo, […] A denúncia foi feita pelos motoristas que fazem o transporte.
Disponível em: http://g1.globo.com/sao-paulo/noticia/2015/03/merendafica-armazenada-ao-lado-de-produtos-quimicos-em-transportadora .html. Acesso em: jan. 2018.
O armazenamento apropriado de produtos, sejam alimentícios ou químicos, tem por finalidade garantir a segurança da saúde e da vida das pessoas. Na organização de um depósito ou almoxarifado, alguns reagentes também não podem ser armazenados junto a outros produtos químicos, pois podem produzir reações perigosas devido à incompatibilidade química, em caso de um acidente.
Assim, para o armazenamento de Produtos Químicos é necessário que:
I. Ácidos e Bases sejam ser estocados em armários diferentes e também separados em sólidos e líquidos.
II. Sais e ácidos fortes sejam armazenados na mesma prateleira, como por exemplo, o cianeto de potássio e ácido clorídrico.
III. Compostos voláteis sejam armazenados dentro da capela de exaustão, para que o ambiente do laboratório não seja contaminado.
IV. Líquidos inflamáveis sejam estocados distantes de fontes de ignição e de produtos oxidantes.
V. Peróxidos estejam distantes de tubulações de água, pois são altamente reativos com esta.
Tendo por base as informações acima, assinale
a alternativa que apresenta as afirmações corretas.
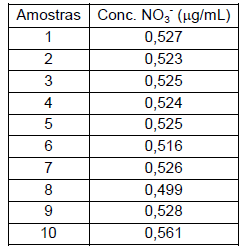
Um Profissional Técnico de Laboratório precisava determinar o teor de cinzas de uma amostra de biodiesel e seguiu uma metodologia descrita por Araújo et al, 2008. Para isso, ele utilizou cadinhos previamente tarados via aquecimento em mufla e pesagem. Nos cadinhos foram adicionados uma determinada quantidade de biodiesel. A seguir, a amostra foi submetida a aquecimento até a temperatura de combustão e após a queima foi aquecida a uma temperatura de 800°C por 2 horas. Em seguida foi adicionada uma solução aquosa de ácido sulfúrico (1:1) e a amostra foi novamente submetida ao processo de aquecimento (800°C por 2 horas). O Profissional Técnico aguardou o resfriamento e efetuou a pesagem dos cadinhos. O procedimento de aquecimento foi repetido até observação de peso constante.
ARAÚJO, A. M. M.; EVANGELISTA, J. P. C.; GOMES, A. F.; SOUZA, L. D.; MATIAS, L.G. O. Análises das cinzas sulfatadas do biodiesel produzido a partir da matéria-prima extraída do RN. In: 48º Congresso Brasileiro de Química – Química na Proteção ao Meio Ambiente e à Saúde. Rio de Janeiro, 2008.
Acerca da situação hipotética descrita acima,
assinale a alternativa correta.
A medição volumétrica é um procedimento muito comum em atividades laboratoriais. Em análises quantitativas, a exatidão e precisão das medidas são de grande importância, fator que pode ser influenciado também pela escolha da vidraria utilizada. Pipetas graduadas, provetas e buretas são alguns exemplos de vidrarias comumente utilizadas em laboratório.
Sobre vidrarias utilizadas em medições
volumétricas, assinale a alternativa correta.
Um professor de química ministrou uma aula sobre toxicidade de metais, na qual foi avaliada a inibição do crescimento da raiz de cebola submersa em soluções de sulfato de cobre em diferentes níveis de concentração.
Para o preparo das soluções, foi utilizada uma solução aquosa de sulfato de cobre a 6,2 x 10-5 mol L-1 , e a mesma foi diluída nas proporções de 1:20, 1:10 e 1:1 (v/v). (Dados: Cu = 63,5 g mol-1 ; S = 32,1 g mol-1 ; e O = 16 g mol-1 ).
Sobre o experimento realizado, assinale a
alternativa correta.
Sobre a reação a seguir é CORRETO afirmar:
AsF3(g) + SbF5(l) → [AsF2]+[SbF6]-
(s)