Questões de Concurso Sobre química
Foram encontradas 14.919 questões
Com relação aos nanomateriais de carbono é INCORRETO afirmar que:
(FIRME, L. P.; VILLANUEVA, F. C. A.; RODELLA, A. A. Solo contaminado com cádmio: extratibilidade do metal e cinética química de degradação da matéria orgânica de torta de filtro. Química Nova, 30 jun. 2014.)
Sobre o metal Cádmio, avalie as frases abaixo e assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
I. Apresenta seus elétrons distribuídos em cinco níveis de energia. II. Seus dois elétrons mais energéticos estão no subnível 5s. III. Seus elétrons de valência apresentam número quântico principal igual a cinco e número quântico do momento angular do orbital igual a zero.
Curare é um nome comum a vários compostos orgânicos venenosos conhecidos como venenos de flecha, extraídos de plantas da América do Sul. Possuem intensa e letal ação paralisante, embora sejam utilizados medicinalmente como relaxante muscular ou anestésico. Um deles é a Tubocurarina, apresentada abaixo.
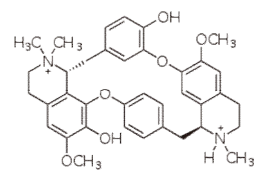
Em sua moléculas podemos visualizar algumas fincões orgânicas, dentre elas a
De acordo com a tabela a seguir

Numa eventual pilha entre os metais mostrados acima, aquele que será sempre o agente redutor é o: