Questões de Concurso Sobre química
Foram encontradas 14.919 questões
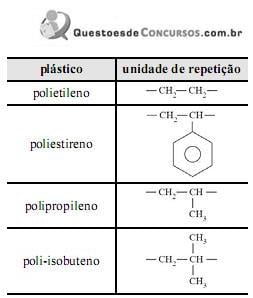
A temperatura de transição vítrea é utilizada para caracterizar inúmeros materiais plásticos. Acerca desse assunto, julgue o seguinte item, considerando a tabela acima.
Quanto à flexibilidade das cadeias poliméricas, o polietileno apresenta menor temperatura de transição vítrea que a do poliestireno.

A temperatura de transição vítrea é utilizada para caracterizar inúmeros materiais plásticos. Acerca desse assunto, julgue o seguinte item, considerando a tabela acima.
Quanto à simetria da unidade de repetição, o poli-isobuteno apresenta maior temperatura de transição vítrea que a do polipropileno.

A temperatura de transição vítrea é utilizada para caracterizar inúmeros materiais plásticos. Acerca desse assunto, julgue o seguinte item, considerando a tabela acima.
A temperatura de transição vítrea é observada em plásticos amorfos e semicristalinos.
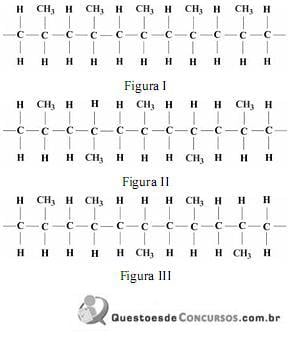
Temperatura de fusão, cristalinidade e solubilidade, que dependem significativamente da estrutura macromolecular dos polímeros, são exemplos de propriedades de elevado interesse de materiais plásticos. Tendo como referência as figuras acima, julgue o item a seguir, acerca da configuração espacial das moléculas do monômero em cadeias de polipropileno.
A configuração isostática, representada na estrutura mostrada na figura I, é caracterizada pelo elevado grau de orientação molecular interna.

Temperatura de fusão, cristalinidade e solubilidade, que dependem significativamente da estrutura macromolecular dos polímeros, são exemplos de propriedades de elevado interesse de materiais plásticos. Tendo como referência as figuras acima, julgue o item a seguir, acerca da configuração espacial das moléculas do monômero em cadeias de polipropileno.
Quanto à taticidade das cadeias poliméricas, a estrutura mostrada na figura III representa uma configuração do tipo sindiotática.

Temperatura de fusão, cristalinidade e solubilidade, que dependem significativamente da estrutura macromolecular dos polímeros, são exemplos de propriedades de elevado interesse de materiais plásticos. Tendo como referência as figuras acima, julgue o item a seguir, acerca da configuração espacial das moléculas do monômero em cadeias de polipropileno.
Plásticos à base de polipropileno puro com isostaticidade acima de 90% são considerados materiais amorfos.
O tetraidrocanabinol (THC), substância que age no sistema nervoso central, é o princípio ativo da maconha.
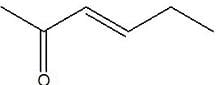
(Dados:NaOH= 40 g/mol)
(Dados:H2 SO4 98 g/mol)
Com base nas informações apresentadas, NÃO se pode concluir que
