Questões de Química - Química Orgânica para Concurso
Foram encontradas 1.987 questões
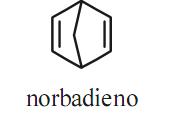
O pesticida aldrin, muito empregado em todo o mundo no combate de pragas, é produzido a partir da reação de Diels-Alder de um composto bicíclico, conhecido como norbadieno, com o hexacloropentadieno. Com relação ao texto, julgue o item subsequente.
O composto norbadieno é obtido por meio da reação de Diels- Alder do ciclopentadieno com o eteno.
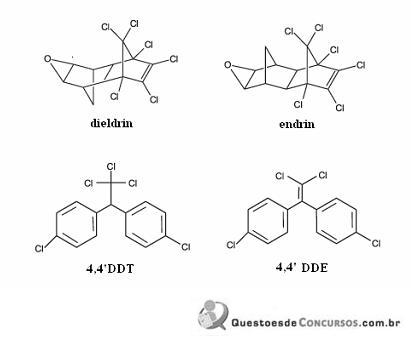
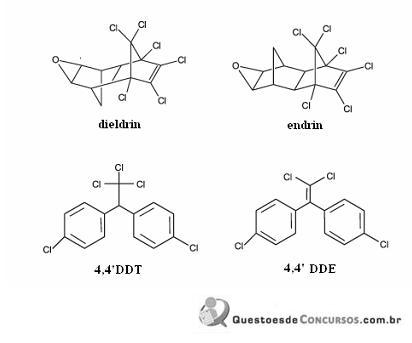
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O dieldrin e o endrin são isômeros constitucionais.
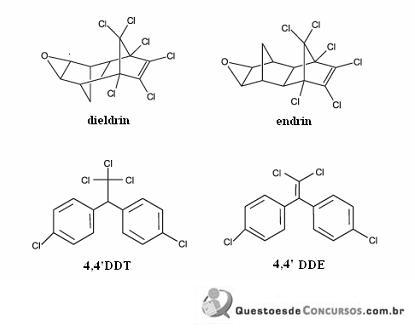
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE denomina-se 1,1-di(p-clorobenzil)-eteno.
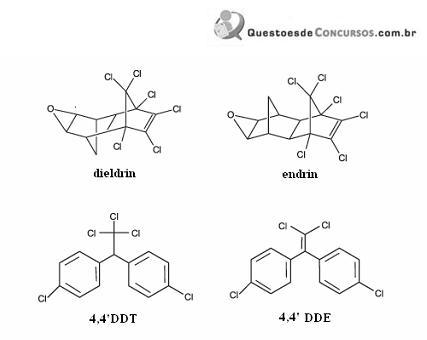
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
A molécula de dieldrin apresenta a função éter.
Considerando a figura acima, que ilustra as estruturas químicas de quatro pesticidas, julgue os itens que se seguem.
O composto 4,4’DDE consiste no principal produto da reação do 4,4’DDT com KOH, que se processa via mecanismo de eliminação bimolecular.
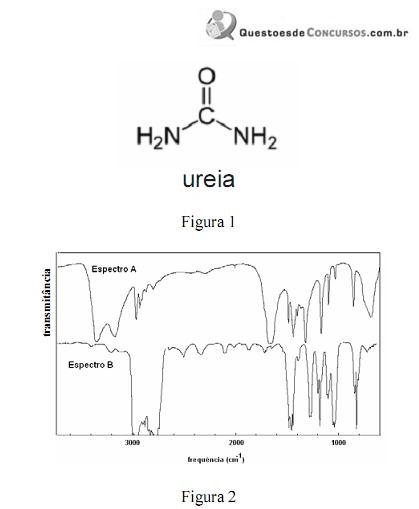
A amônia serve como substrato para a síntese de um grande número de substâncias, como aminas e amidas. Merece destaque a ureia, que é largamente empregada como fertilizante e cuja estrutura é apresentada na figura 1. Na figura 2, são apresentados os espectros de infravermelho de duas outras substâncias que podem ser sintetizadas a partir da amônia: a propanamida e a trietilamina, sendo que os espectros não estão apresentados, necessariamente, nessa ordem. Com relação aos derivados da amônia citados e aos espectros apresentados, julgue os itens que se seguem.
A ureia apresenta basicidade mais elevada que a amônia.
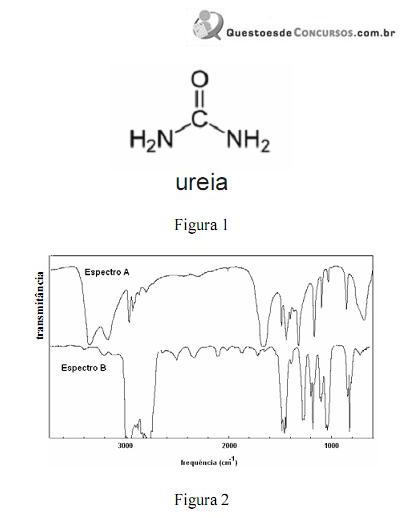
A amônia serve como substrato para a síntese de um grande número de substâncias, como aminas e amidas. Merece destaque a ureia, que é largamente empregada como fertilizante e cuja estrutura é apresentada na figura 1. Na figura 2, são apresentados os espectros de infravermelho de duas outras substâncias que podem ser sintetizadas a partir da amônia: a propanamida e a trietilamina, sendo que os espectros não estão apresentados, necessariamente, nessa ordem. Com relação aos derivados da amônia citados e aos espectros apresentados, julgue os itens que se seguem.
A etilamina apresenta ponto de ebulição menor que o etanol.
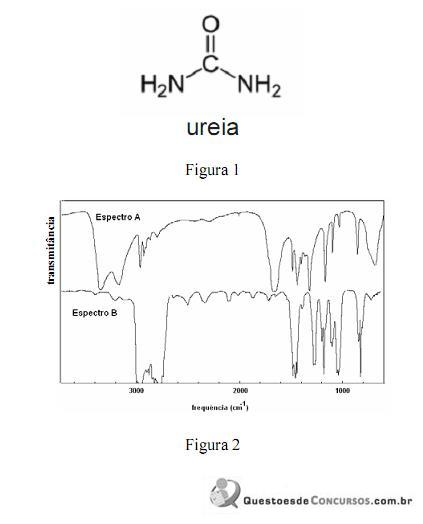
A amônia serve como substrato para a síntese de um grande número de substâncias, como aminas e amidas. Merece destaque a ureia, que é largamente empregada como fertilizante e cuja estrutura é apresentada na figura 1. Na figura 2, são apresentados os espectros de infravermelho de duas outras substâncias que podem ser sintetizadas a partir da amônia: a propanamida e a trietilamina, sendo que os espectros não estão apresentados, necessariamente, nessa ordem. Com relação aos derivados da amônia citados e aos espectros apresentados, julgue os itens que se seguem.
A reação da amônia com a propanona resulta na formação da etanamida.
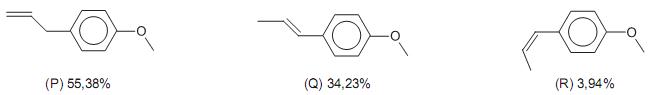
Disponível em: http://teses.icict.? ocruz.br/pdf/paulajfpm.pdf
Acesso em: 08 out. 2010. (Adaptado)
Em relação a algumas reações que podem ser realizadas com o estragol, transanetol e cisanetol, analise as afirmativas a seguir.
I - Os produtos principais da reação de hidrogenação de (P) e (Q), catalisada por platina a 25 °C e a pressão de 1 atm, são isômeros constitucionais.
II - Tanto (Q) como (R) podem descorar uma solução de
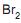 em tetracloreto de carbono com a formação de um mesmo produto principal de reação.
em tetracloreto de carbono com a formação de um mesmo produto principal de reação. III - A reação de (P) com HBr pode levar a formação de um produto de reação idêntico ao obtido na reação de (Q) com HBr.
IV - O calor liberado na reação de hidrogenação da dupla olefínica de (Q) é menor do que na de (R).
Estão corretas APENAS as afirmações
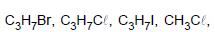
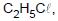 em ordem crescente de ponto de ebulição são:
em ordem crescente de ponto de ebulição são: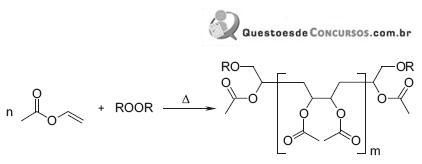
Em relação a este processo, é correto afirmar que
I - Copolímeros consistem em uma mistura física de dois homopolímeros compostos por monômeros estruturalmente diferentes, normalmente pela mistura de soluções dos dois polímeros, seguida da evaporação do solvente.
II - Copolímeros podem ser obtidos pela reação entre diferentes monômeros, sendo que a proporção relativa entre eles na estrutura do copolímero dependerá de suas reatividades químicas.
III - Copolímeros, por possuírem mais de um monômero, apresentarão as propriedades físicas e químicas dos homopolímeros, combinadas em um único material.
É(São) correta(s) APENAS a(s) afirmativa(s)
P0 acetona = 345 torr P0 clorofórmio = 295 torr
Sobre isomeria constitucional assinale a opção INCORRETA abaixo:
A desoxirribose, pentose presente na molécula de DNA, apresenta fórmula estrutural:
A cadeia carbônica acima representada pode ser classificada como:
A importância do uso da medicação correta durante um quadro de dengue é fundamental para a melhora do paciente e para a prevenção de complicações. Por exemplo, em casos de suspeita de dengue, o uso de medicamentos como o AAS (ácido acetilsalicílico) deve ser evitado devido ao risco de complicações hemorrágicas. O AAS é classificado como sendo um analgésico e antitérmico e possui fórmula estrutural mostrada abaixo:
Considerando a fórmula estrutural do ácido acetilsalicílico, assinale a alternativa CORRETA que apresenta sua fórmula molecular e os grupos funcionais orgânicos presentes na estrutura.
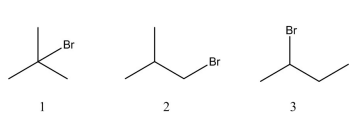
Dadas as afirmativas referentes aos espectros obtidos dos bromoalcanos isoméricos,
I. O espectro obtido a partir do composto 1 apresenta um único sinal.
II. O composto 2 gera um espectro que contém quatros sinais distintos.
III. A análise da amostra contendo o 2-bromobutano ( composto 3) mostra dois multipletos: um dupleto e um tripleto.
IV. O hidrogênio metínico do composto 2 gera um tripleto no espectro.
verifica-se que está/ão correta/s