Questões de Concurso
Comentadas sobre sistemas homogêneos: constantes: kc e kp. deslocamento do equilíbrio: fatores. em química
Foram encontradas 69 questões
O SO2Cl2 (g) decompõe-se facilmente de acordo com aequação:
SO2Cl2 (g) ⇌ SO2 (g) + Cl2 (g) ΔH > 0
Por esse motivo, ele é muito empregado como fonte deCl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa
reação apresentem comportamento ideal e que a lei de velocidade
para a reação seja dada pela equação v = k × [SO2Cl2]. Considere
também que, na temperatura em que a reação ocorre (T), a
constante de equilíbrio (Keq) da reação valha 0,40.
Com base nesses dados, assinale a alternativa que mostra o valor da constante Kc para essa reação.
Acerca de equilíbrio químico, julgue o item subsequente.
O princípio de Le Châtelier permite prever como a mudança
da pressão afetaria o equilíbrio de uma reação química.
Acerca de equilíbrio químico, julgue o item subsequente.
Considere que, para a reação
2 NOCl (g) ⇌ 2 NO (g) + Cl2 (g), ocorrendo a 796 ℃, a
constante de equilíbrio com base nas concentrações valha
Kc = 3,75 × 10−6 e que a constante universal dos gases
perfeitos valha 0,082 L · atm · K−1 · mol−1. Nesse caso, a
constante de equilíbrio com base nas pressões parciais, Kp, é
inferior a 1 × 10−4.
O chumbo metálico pode ser produzido pela redução de minério de chumbo com coque em reator com controle de pressão, em um processo reversível conforme a equação química a seguir, cuja variação de entalpia nas condições padrão é igual a 42 kJ/mol.
2 PbO (s) + C (s) ⇌ 2 Pb (s) + CO2 (g)
Nessas condições, o rendimento do processo em quantidade de matéria pode ser aumentado pela
Sabendo-se que a nova mistura tem constante de equilíbrio igual a 4, após o novo equilíbrio ser alcançado, a quantidade de acetato será de:
CO (g) + CL2 (g) → COCl2 (g)
Sabendo que o grau de equilíbrio é 80%, o cálculo de Kc para esse experimento deverá apresentar o resultado aproximado de
O íon complexo [Zn(NH3)]+2 é formado a partir 3 4 da seguinte reação química:
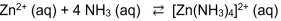
Em um experimento, ao se atingir o equilíbrio químico, as concentrações dos participantes da reação são apresentadas na tabela a seguir.
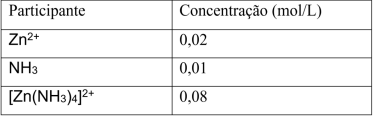
A constante de equilíbrio dessa reação é igual a:

Para melhorar o rendimento dessa síntese, duas modificações podem ser feitas sobre o sistema:
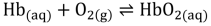
(Onde Hb é a hemoglobina e HbO é oxi- 2 hemoglobina.) O rendimento físico de um atleta está ligado, entre outros fatores, à capacidade de metabolizar oxigênio, o que pode ser prejudicado pela altitude na qual a atividade física está sendo realizada. Assim, um atleta acostumado a treinar no Rio de Janeiro (nível do mar) tem seus resultados físicos prejudicados quando compete na Cidade do México (2250 m acima do nível do mar) pois, nessa altitude, a pressão:
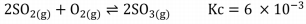
Considerando que a reação foi mantida em um recipiente de 2 L a 300K e as quantidades de dióxido de enxofre e de oxigênio no equilíbrio são 0,2 e 1,2 mols respectivamente, a concentração molar do produto obtido no equilíbrio é de:
Fe2O3 (s) + x H+ (aq) ⇌ y Fe3+ (aq) + z H2O (l)
Com base nessas informações, julgue o seguinte item.
A constante de equilíbrio K da reação do óxido de ferro (III) é corretamente expressa pela seguinte equação. K = [ Fe3+ ]y [ H20]z / [Fe2O3] [ H+]x
3 Cuo(s) + 8 HNO3(aq) → 3 Cu(NO3)2(aq) + 2 NO(g) + 4 H2O(l) (1) 2 NO(g) + O2(g) → 2 NO2(g) (2) NO2(g) ⇌ N2O4(g) (3)
Isso posto, considerando um sistema transparente e fechado, o produto NO2(g) apresenta coloração marrom. O produto N2O4(g) é um gás incolor e, quando o sistema é aquecido acima da temperatura ambiente, o sistema apresenta uma coloração marrom (forte). Em relação à equação três, referente à formação do N2O4(g), é correto afirmar que:
As reações a seguir representam o sistema de tamponamento sanguíneo do bicarbonato.
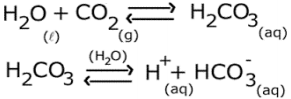
De acordo com as reações, o aumento de CO2 no sangue
resulta em
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
As expressões da constante de equilíbrio são muito
importantes porque permitem que os químicos possam
prever a direção e a extensão de uma reação química.
Contudo, uma expressão da constante de equilíbrio não
fornece informações relacionadas à velocidade na qual
o equilíbrio é alcançado.
Com relação à velocidade de reação química, a fatores que a influenciam e a assuntos correlatos, julgue o item
Pelo princípio de Le Chatelier, quando se exerce uma
ação sobre um sistema em equilíbrio dinâmico, ele se
desloca no sentido que produz uma minimização da ação
exercida. Em outras palavras, sempre que se aplicar um
esforço sobre um sistema em equilíbrio, a posição de
equilíbrio será alterada na direção que tende a
minimizar ou anular o efeito do esforço aplicado.
[PCl5 ] 0,0456 Mol. L-1 [PCl3 ] 0,0211 Mol. L-1 [Cl2 ] 0,0121 Mol. L-1
Calcule o valor da constante de equilíbrio (em termos da concentração) em 170°C.
[H2]=1,83x10-3 mol/L, [l2]= 3, 12x10-3 mol/L e [HI]= 17,67 X 10-3 mol/L. 2 HI(g)
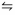 H2(g) + I2(g)
H2(g) + I2(g)Em um experimento, avaliou-se a seguinte reação química:

As concentrações iniciais de SO2 e O2 foram 0,3 mol/L e 0,2 mol/L, respectivamente. No início da reação, não havia SO3 no reator, mas atingido o equilíbrio, sua concentração foi igual a 0,2 mol/L.
Para esse sistema, a constante de equilíbrio, em termos
de concentrações, é igual a