Questões de Concurso
Comentadas sobre substâncias inorgânicas e suas características: ácidos, bases, sais e óxidos. reações de neutralização. em química
Foram encontradas 137 questões
Qual a concentração da solução de hidróxido de potássio para neutralizar completamente o ácido?
Considere a massa molar do HNO3 igual a 63 g/mol e a massa molar do KOH igual a 56 g/mol.
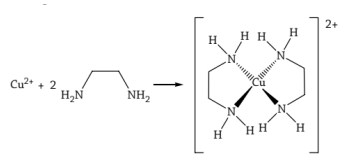
Fonte: https://www2.ufjf.br/quimicaead/wp - content/uploads/sites/224/2013/09/QI_Aula4
O indicador recomendado para determinar o ponto final dessa titulação é o(a)
O reagente recomendado para esse tratamento preliminar da amostra é o
Para realizar o correto descarte da solução titulada citada em III, são indicados a neutralização com bases e o descarte lento na pia, sob água corrente.
Nos estudos de Alessandro Volta, que tomou como base os experimentos e as teorias de Galvani, foram utilizados diferentes discos de metais (Cu/Sn ou Zn/Ag) empilhados e conectados com pedaços de papel umedecidos em solução salina. Dessa maneira, o cientista conseguiu encontrar o método para a geração de corrente elétrica e estabeleceu evidências para a existência da eletricidade por meio da construção da pilha — cujo nome vem do empilhamento dos discos. Na tabela a seguir, são mostrados os potenciais padrão de redução de algumas espécies químicas em água.

Entre os metais apresentados na tabela, o ferro é o mais facilmente oxidável.
Internet: <g1.globo.com> (com adaptações).
Considerando as informações do texto anterior, julgue o item subsequente.
O anidrido bórico é um óxido obtido a partir da retirada total de moléculas de água da estrutura do ácido bórico e possui fórmula molecular BO3.
Internet: <g1.globo.com> (com adaptações).
Considerando as informações do texto anterior, julgue o item subsequente.
A reação de neutralização parcial entre o ácido bórico e o hidróxido de cálcio na proporção de 1:1 pode formar o mono-hidrogenoborato de cálcio e duas moléculas de água.
Coluna 1 1. CaO 2. H2SO4 3. CO2 4. H3PO4 5. BeO
Coluna 2 ( ) Óxido ácido. ( ) Óxido anfótero. ( ) Óxido básico. ( ) Ácido poliprótico. ( ) Ácido diprótico.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Com relação às propriedades de tais substâncias, e considerando a teoria de Arrhenius, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Em solução aquosa, ácidos liberam prótons H+ e bases liberam ânions H- . ( ) Quando colocados em água, ácidos sofrem ionização e bases, dissociação iônica. ( ) Os ácidos são líquidos corrosivos e perigosos, por isso não podem entrar em contato com a pele nem ser ingeridos.
As afirmativas são, respectivamente,
2HCl (aq) + CaCO3 (s) → CaCl2 (aq) + H2O (l) + CO2 (g)
Pensando nas condições normais de temperatura e pressão (CNTP), vamos calcular a massa de água, em gramas, e o volume de gás carbônico, que pode se formar a partir de 80g de carbonato de cálcio. Dados as massas atômicas de Ca= 40; C = 12; O=16. Assinale a alternativa que apresenta os valores encontrados.
O Regulamento Técnico SVS/MS nº 540/1997 considera o fermento químico como um aditivo, e como tal, necessita obrigatoriamente ser registrado na ANVISA de acordo com as orientações da Resolução nº 23 (ANVISA, 2000).
Basicamente, os fermentos químicos são constituídos de uma mistura de pirofosfato ácido de sódio, bicarbonato de sódio e fécula de mandioca. Além do conhecido bicarbonato de sódio, assinale a alternativa que apresente alguns ácidos que podem fazer parte da composição.
O SO2 (g) é um óxido ácido.
O aumento do pH da água é provocado por um ácido.
Na reação apresentada no texto, o ácido H2S é o agente oxidante.