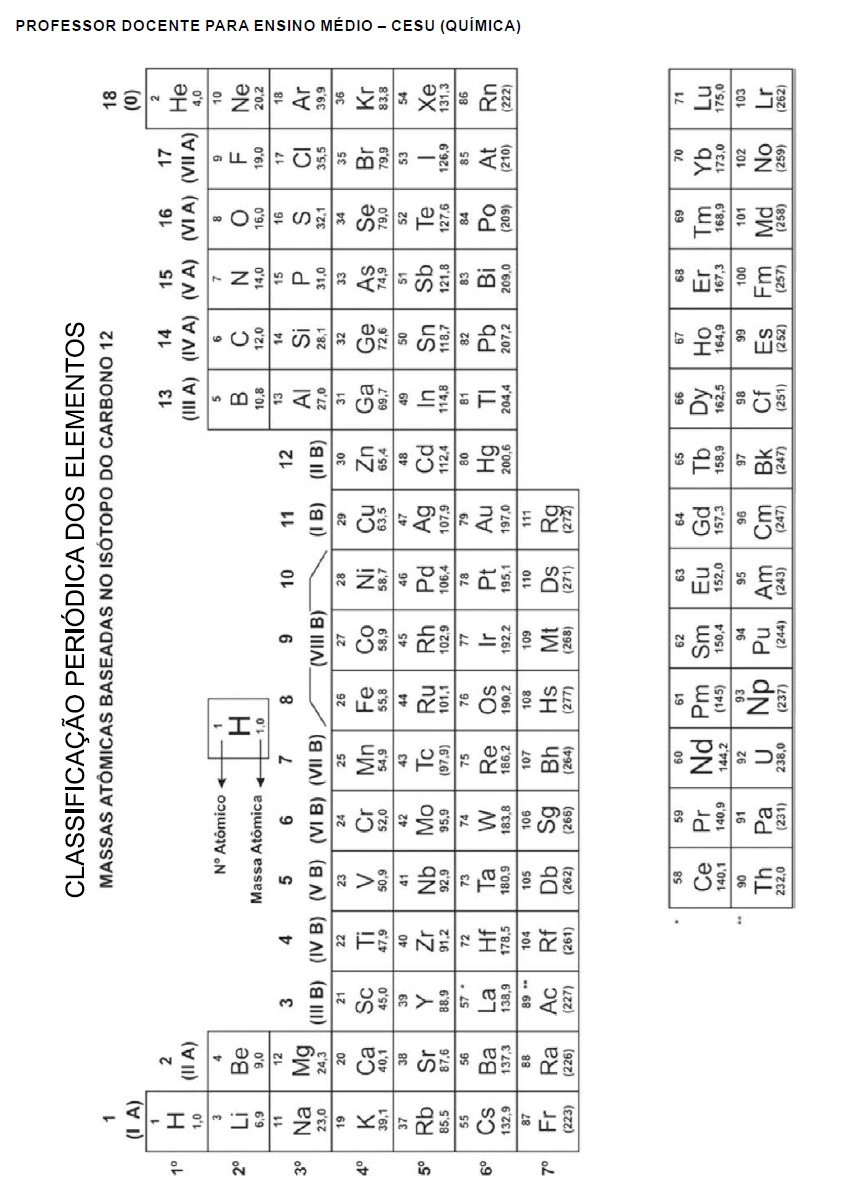
Questões de Química - Teoria Atômica: átomos e sua estrutura - número atômico, número de massa, isótopos, massa atômica para Concurso
Foram encontradas 373 questões
T = 19 prótons e 21 nêutrons.
X = 19 prótons e 20 nêutrons.
Y = 20 prótons e 19 nêutrons.
Z = 20 prótons e 20 nêutrons.
Com base nessas afirmações, assinale a alternativa correta.
X: 1s2 Y: 1s2 2s2 2p5 Z: 1s2 2s2 2p6 3s2 3p5
Com relação a esses elementos químicos (X, Y e Z), as seguintes afirmações foram feitas:
1) X apresenta a maior energia de ionização. 2) Y e Z apresentam o mesmo raio atômico. 3) Y e Z pertencem ao mesmo grupo da Tabela Periódica.
Está(ão) correta(s) a(s) afirmativa(s):
Leia atentamente os textos 1 e 2: Texto 1: “Em 1869, um professor da Universidade de São Petersburgo, o russo Dmitri Mendeleev (1834–1907), concebeu um diagrama em que ordenava cerca de 60 elementos químicos então conhecidos em função de sua respectiva massa. Essa foi a primeira versão do que viria a ser conhecida como a moderna tabela periódica, hoje composta de 118 elementos, dispostos em 18 grupos (colunas) e 7 períodos (linhas).”
Fonte: Disponível em: https://revistapesquisa.fapesp.br/2019/03/14/a-encruzilhadada-tabela-periodica/. Acesso em 19 jun. 2019). 18
Texto 2:
“Você já ouviu falar do ununênio? Ununênio, ou mesmo Eka-Frâncio, é como se chama, provisoriamente, aquele que será o elemento de número atômico 119 da tabela periódica. Ele se localizará na família dos metais alcalinos, se assemelhando ao lítio, sódio, potássio, rubídio, césio, e frâncio, sendo responsável por iniciar o oitavo período da tabela de Henry Moseley e representado pelo símbolo Uue.”
Fonte: Disponível em: http://www.petquimica.ufc.br/ununenio-um-elemento-aindanao-sintetizado/. Acesso em 19 jun. 2019
Os textos 1 e 2 referem-se à disposição dos elementos químicos inseridos nos
últimos anos na atual Tabela Periódica e mencionam que estes encontram-se,
respectivamente, nos 7º e 8º períodos. Indique a alternativa abaixo que melhor
define os períodos na Tabela Periódica:
Sobre as propriedades periódicas dos elementos, assinale a alternativa incorreta.
Analise as afirmativas a seguir:
1. A massa atômica de certo elemento que é apresentada na tabela periódica corresponde à média ponderal das massas atômicas dos seus isótopos naturais.
2. Os nêutrons são partículas subatômicas com carga positiva e têm aproximadamente a mesma massa do elétron.
3. Os isótopos de um elemento têm o mesmo número atômico, mas diferentes números de massa.
4. Para um elemento neutro, a soma do número de prótons e de nêutrons corresponde ao seu número de massa.
5. A disposição dos elementos na tabela periódica está baseada no número atômico do elemento que corresponde à soma dos seus prótons e de seus elétrons.
Assinale a alternativa que indica todas as afirmativas corretas.