Questões de Química - Transformações Químicas e Energia para Concurso
Foram encontradas 1.412 questões
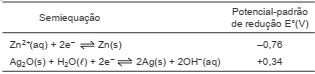
A pilha de zinco e óxido de prata é usada em aparelhos auditivos e relógios de pulso e são menos poluentes do que a de zinco e óxido de mercúrio.
Tendo em vista essas informações e os dados da tabela de
potencial-padrão de redução para as semiequações que
ocorrem nessa pilha, é correto afirmar:
Cr2O2-7 (aq) + Cℓ− (aq) + H+ (aq) → Cr3+(aq) + H2O(ℓ) + Cℓ2(g)
No balanceamento de equações de oxirredução, algumas espécies transferem elétrons para outras, de forma que, no final da reação química, o número de elétrons transferidos é igual ao de elétrons recebidos.
Com base nessas informações e após o balanceamento da equação química com os menores coeficientes estequiométricos inteiros, é correto afirmar:
I. 2H+(aq) + 1/2O2(aq) + 2e- → H2O(ℓ) Eºred = + 1,23v
II. Fe3+(aq) + e- → Fe2+(aq) Eºred = +0,77
As soluções aquosas ácidas de sais de íons Fe2+(aq) são esverdeadas quando recém-preparadas e, quando em contato prolongado com o ar, tornam-se amareladas.
A partir dessas considerações e das semiequações I e II
com os respectivos potenciais-padrão de redução, é correto
afirmar:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ΔHo = − 890kJ
A energia elétrica proveniente de biomassa é uma alternativa amplamente utilizada por grandes empresas do agronegócio nas regiões sul e sudoeste. A energia produzida não somente atende às necessidades dos empreendimentos, como também é vendida a concessionárias na região. A fermentação de restos de vegetais e de dejetos de animais coletados nas fazendas de pecuária e de suinocultura é processada em biodigestores e produz biogás, uma mistura gasosa de metano, CH4(g), sulfeto de hidrogênio, H2S(g) e dióxido de carbono, CO2(g), dentre outros gases, e resíduos ricos em bionutrientes usados como fertilizantes na propriedade rural. A combustão do metano, mostrada pela equação química, libera calor utilizado na geração de energia elétrica.
De acordo com essas informações sobre o processo de
geração de energia a partir de biomassa, e
considerando-se o calor específico da água 4,2Jg−1
K−1
, é
correto afirmar:
Reação de combustão do metano:
CH4(g) + 2 O2(g) → CO2(g) + 2 H2 O(g) ΔH = - 890,4 kJ/mol