Questões de Química - Transformações Químicas e Energia para Concurso
Foram encontradas 1.424 questões
Com relação a decaimento, considere as seguintes equações:
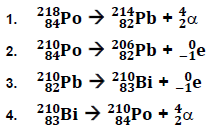
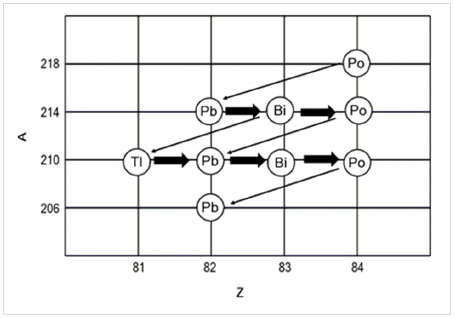
São equações de decaimento:
Para a remoção de cromo hexavalente (Cr6+) pode-se utilizar dióxido de enxofre (SO2). A redução do Cr6+ se dá em meio ácido com pH entre 2 e 3. Após a neutralização com hidróxido de cálcio [Ca(OH)2], em pH 8 a 9, o cromo precipita como hidróxido de cromo III (Cr(OH)3). As reações envolvidas são:
− Redução: 3 SO2 + 2 H2CrO4 + 3 H2O → Cr2(SO4)3 + 5 H2O
− Precipitação: Cr2(SO4)3 + 3 Ca(OH)2 → 2 Cr(OH)3 + 3 CaSO4
− Estequiometricamente é necessário na redução 2,0 g de SO2/g Cr6+ e de 2,0 g de H2SO4 / g Cr6+
− Na precipitação utiliza-se 2,6 g de Ca(OH)2 /g Cr6+
Para tratar um efluente de 8,0 m3 contendo 0,50 g de g Cr6+/L de efluente, o consumo de SO2, H2SO2 e Ca(OH)2 são, respectivamente:
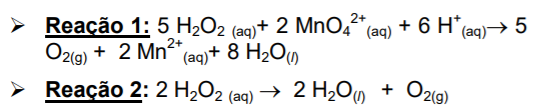
Com relação às informações dadas, podemos afirmar que:
I. A determinação de peróxido é um método complexiométrico. II. A expressão da concentração, em volumes decorre da auto protólise do peróxido. III. Na reação de permanganometria, o peróxido de hidrogênio é o agente redutor. IV. Para este procedimento deve ser empregado um indicador metalocrômico. V. A expressão “volumes de água oxigenada” se deve à geração de oxigênio na sua decomposição.
Estão CORRETAS apenas as afirmativas:
Fe+2(aq) + 2 e- → Fe(s) E° = - 0,44 V Pb+2(aq) + 2 e- → Pb(s) E°= - 0,13 V
E considerando a formação de uma pilha, são feitas as seguintes afirmativas:
I. A reação que ocorre no cátodo é Pb+2(aq) + 2 e- → Pb(s). II. A Pilha pode ser representada por Fe2+(aq) / Fe(s) // Pb2+(aq) / Pb(s). III. A voltagem da pilha é igual a 0,31 V. IV. A reação não é espontânea.
Assinale a alternativa em que todas as afirmativas estão CORRETAS:
___ P + ___ HNO3 + __ H2O →__ H3PO4 + 5 NO
Após balanceamento, a soma dos coeficientes estequiométricos dos reagentes é __________. Nesta reação, o __________sofre oxidação e o __________sofre redução.
Assinale a alternativa que apresenta as palavras que preenchem CORRETAMENTE as lacunas, na ordem em que aparecem no texto: