Questões de Concurso
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 1.107 questões
Elementos Químicos Distribuição Eletrônica
I 1s2 2s2 2p6 3s23p3 II 1s2 2s2 2p6 3s2 3p6 4s2 3d8 III 1s2 2s2 2p6 3s2 3p6 4s2 IV 1s2 2s2 2p6 3s2 3p6 4s23d10 4p3 V 1s2 2s2 2p6 3s2 3p
De acordo com as informações localizadas na tabela acima, é correto afirmar que:
A tabela periódica dos elementos químicos relaciona os elementos em linhas (Períodos) e colunas (Grupos ou Famílias), dispostos em ordem crescente de seus números atômicos. As propriedades dos elementos químicos presentes no mesmo grupo são semelhantes. Neste contexto, considere os seguintes elementos químicos e seus respectivos números atômicos.
Césio (Cs) Z = 55
Enxofre (S) Z = 16
Argônio (Ar) Z = 18
Magnésio Mg) Z =12
A partir dessas informações assinale a
alternativa correta.
As reações abaixo representadas por I, II e III podem ser classificadas, respectivamente, como reações de:
I. N2O4(g) → 2 NO2(g)
II. 2 Cr(s) + 3 PbSO4(aq) → Cr2 (SO4 )3(aq) + 3 Pb(s)
III. 3 Ca(OH)2(aq) + Al2
(SO4
)3(s) → 2 Al(OH)3(aq) + 3 CaSO4(s)
Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão de Química.
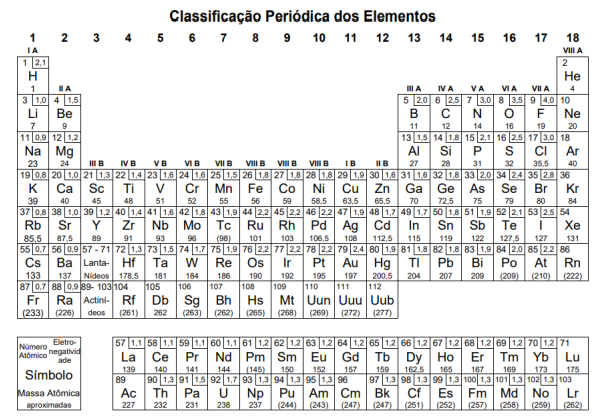
Sobre esses três elementos, avalie as seguintes afirmações:
I. Bário é um metal alcalino terroso.
II. Antimônio é o que possui maior raio atômico.
III. Chumbo possui quatro elétrons na sua camada de valência.
Está correto apenas o que se afirma em
No que tange à química geral e à inorgânica, julgue o item seguinte.
A reação de substituição ocorre quando duas substâncias
compostas trocam seus elementos, formando-se, assim,
novas substâncias.
No que tange à química geral e à inorgânica, julgue o item seguinte.
As reações químicas ocorrem sem a presença de fator
externo.
I. possuem baixos ponto de fusão, ponto de ebulição e densidade. II. reagem violentamente com água, gerando como produtos uma base e gás hidrogênio. III. perdem elétrons com facilidade, tendendo a formar íons monovalentes.
Possuem essas características os elementos químicos pertencentes ao grupo
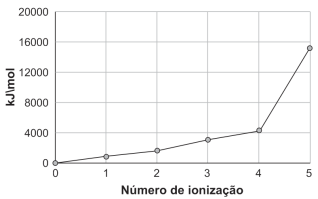
De acordo com as informações, o elemento X é o
Apenas uma pequena parte dos elementos da tabela periódica refere-se aos metais, por serem bons condutores de calor e eletricidade, diferentemente dos ametais, que apresentam má condução de eletricidade e calor. A União Internacional de Química Pura e Aplicada (IUPAC) reconhece o grupo de metaloides, distinguindo-os dos metais por causa de suas propriedades eletrônicas.
Durante os anos de 1800 a 1900, os cientistas da época notaram que muitos dos elementos químicos apresentavam propriedades semelhantes entre si. A observação da regularidade periódica das propriedades físicas e químicas dos elementos conhecidos, bem como a necessidade de organizar um grande volume de informações disponíveis, levaram ao desenvolvimento da tabela periódica.
Gases nobres são átomos encontrados combinados na natureza; qualquer outro átomo, dos demais elementos químicos, geralmente é encontrado isolado, podendo formar inúmeros compostos, sendo que as ligações químicas que mantêm os átomos unidos são fundamentalmente de natureza elétrica.
As reações químicas ocorrem em um nível atômico; no entanto, alguns sinais podem ser observados como indicativo da ocorrência de uma transformação química. Algumas evidências que podem ser percebidas pelos sentidos dos seres humanos são a liberação de energia, a liberação de gases e mudanças de cor.
A alquimia consiste em um conjunto de práticas científicas padronizadas da Idade Média que buscavam a transformação de metais menos nobres em ouro; a transição das técnicas modernas da teoria científica da alquimia à química é reconhecida como a origem da química moderna.
A história da química pode ser plenamente observada sem se considerar a história da filosofia, da educação, das religiões e das artes, por se tratar de uma ciência distinta das demais em termos do seu desenvolvimento histórico.

Considerando essas informações e os diversos aspectos a elas relacionados, julgue o item.
O íon Fe3+ (ZFe= 26) apresenta a mesma configuração
eletrônica que o íon Mn2+ (ZMn = 25).
( ) A carga nuclear efetiva aumenta da esquerda para a direita em qualquer período da tabela periódica. ( ) Em um grupo, a carga nuclear efetiva que atua sobre os elétrons de valência varia muito menos do que em um período da tabela periódica. ( ) A carga nuclear efetiva diminui ligeiramente de cima para baixo em um grupo da tabela periódica. ( ) A carga nuclear efetiva que atua sobre os elétrons da camada mais externa é maior do que aquela que atua sobre os elétrons internos por causa da blindagem exercida pelos elétrons internos.
Assinale a sequência correta.