Questões de Concurso Público SEGEP-MA 2016 para Analista Ambiental – Químico
Foram encontradas 10 questões
Considere a reação 5 Fe2+ + MnO4− + 8H+ → 5 Fe3+ + Mn2+ + 4 H2O utilizada em uma titulação redox para determinação do teor de ferro em 2 g de uma amostra de minério contendo ferro. Nessa titulação foram gastos 47,5 mL de solução 0,02 mol . L−1 de KMnO4 para alcançar o ponto de equivalência. A porcentagem em massa de ferro na amostra é
Dados:
Massas molares (g . mol−1)
K = 39;
Fe = 56;
Mn = 55; O = 16;
H = 1
O quadro abaixo representa os equilíbrios ácido-base entre o ácido sulfuroso e amônia em solução aquosa.
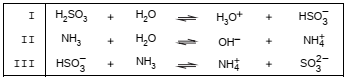
De acordo com a teoria de Brönsted-Lowry,
Deseja-se dessalinizar 1 m3 de água do mar a 25 °C. A pressão osmótica (em atm) a ser aplicada no sistema dessalinizador, considerando-se apenas os íons Na+ e Cℓ − presentes nessa água, é
Dados:
Constante universal dos gases: 0,082 atm . L . mol−1 . K−1
Concentração do sal na água do mar a 25 °C = 2,95 g.L−1
Massas molares (g . mol−1): Na = 23; Cℓ = 35,5
Considerar o NaCℓ totalmente ionizado para cálculo da constante de Van’t Hoff.