Questões de Concurso Público UFC 2017 para Médico - Pesquisa Clínica
Foram encontradas 50 questões
Considere e analise as afirmativas sobre pesquisa clínica, verifique se são verdadeiras e, em seguida, assinale a alternativa correta.
I. Pesquisa clínica, ensaio clínico ou estudo clínico são termos utilizados para denominar um processo de investigação científica envolvendo seres humanos, ou seja, é um estudo científico para verificar como funcionam uma nova medicação ou um novo procedimento, como, por exemplo, uma nova técnica para sondagem nasogástrica em humano.
II. Ao desenvolver uma nova técnica, como um exame de sangue ou dispositivo de imagem, precisamos de voluntários de pesquisa clínica para ajudar a definir os limites do normal.
III. Em se tratando de pesquisa clínica desenvolvida no Brasil na área oncológica, são autoridades regulatórias: o CEP, a ANVISA e o INCA.
IV. Caso um paciente de 32 anos de idade, com diagnóstico médico de câncer de pâncreas em estágio avançado e com metástase hepática, considerado fora de possibilidade terapêutica, seja incluído em pesquisa clínica, esse indivíduo será considerado um sujeito vulnerável.
V. Uma pesquisa clínica pode conter vários tipos de investigação em estudo, sendo que cada esquema terapêutico é denominado braço. Nesse caso, alguns pacientes que não alcançarem resposta completa ou parcial com um tratamento poderão cruzar (crossover) ou mudar para outro braço do estudo. O pesquisador deve estar atento a tal evento e denunciá-lo às instâncias regulatórias, uma vez que o prejuízo do paciente será notório, principalmente no que concerne ao acúmulo de toxicidades decorrente dos tratamentos sequenciais aos quais o sujeito fica exposto.
O correto está em:
Cada ensaio clínico tem requisitos específicos para quem pode ou não participar. Podemos, então, afirmar que:
I. Os critérios de inclusão e exclusão podem fornecer dados da adequação do sujeito para o estudo, e minimizar a retirada dos participantes da pesquisa, reduzindo, desta forma, os custos financeiros.
II. Os critérios de exclusão indicam o subgrupo de indivíduos que não preenchem os critérios de inclusão, e que também apresenta características ou manifestações que podem interferir na qualidade dos dados, assim como na interpretação dos resultados.
III. Alguns critérios de exclusão podem ser definidos por considerações éticas, outros pela menor disposição de determinados pacientes em participarem do estudo.
IV. Os critérios de inclusão definem as principais características da população alvo e acessível.
V. Os critérios de inclusão e exclusão visam assegurar a segurança dos pacientes durante o estudo.
O correto está em:
No controle de qualidade da pesquisa clínica é correto afirmar que:
I. São técnicas e atividades operacionais desempenhadas dentro do sistema de garantia de qualidade para confirmar que as exigências de qualidade das atividades relativas ao estudo foram cumpridas.
II. Deve ser aplicado a cada estágio de manuseio de dados para assegurar que todos os dados sejam confiáveis e tenham sido processados de forma correta.
III. O patrocinador é responsável por implementar e manter sistemas de garantia de qualidade e controle de qualidade com procedimentos operacionais padrão (POPs) por escrito para assegurar que os ensaios clínicos serão conduzidos e os dados sejam gerados, documentados (registrados) e relatados em consonância com o protocolo, as Boas Práticas Clínicas e as exigências regulatórias aplicáveis.
IV. Um patrocinador pode transferir qualquer uma ou todas as tarefas e funções do mesmo relativas ao ensaio clínico à uma Organização Representativa de Pesquisa Clínica (ORPC). a ORPC deve implementar garantia e controle de qualidade e ter a responsabilidade definitiva pela qualidade e integridade dos dados da pesquisa.
O correto está em:
Na elaboração de fichas clínicas de coleta de dados, ou formulário de relato de caso (CRF), podemos afirmar que:
I. É um documento da pesquisa clínica e deve ser elaborado de acordo com a conformidade do protocolo do estudo. O CRF pode ser um documento impresso ou eletrônico.
II. A concepção de um CRF é crucial num ensaio clínico, uma vez que irá auxiliar na avaliação da segurança e eficácia do medicamento com precisão.
III. Os dados devem ser organizados em um formato que facilite e simplifique a análise de dados. A coleta de grande quantidade de dados resultará em desperdício de recursos na coleta e processamento e em muitas circunstâncias, não será utilizada para análise.
IV. No atual cenário global de pesquisa clínica os CRFs eletrônicos (eCRFs) são preferidos aos CRFs impressos.
V. O CRF eletrônico é projetado de tal forma que a entrada de dados pode ser feita com zero / erros mínimos. Além disso, as autoridades reguladoras aceitam prontamente as propostas em que são utilizados sistemas de captura electrónica de dados validados.
O correto está em:
Na pesquisa clínica com portadores de doenças crônicas podemos afirmar:
I. A partir da homologação de resolução do Conselho Nacional de Saúde, determinou-se a legitimidade da utilização de placebo em grupo-controle quando o estudo possuir finalidade confirmatória terapêutica em caso de doença crônica degenerativa.
II. É permitido aos pacientes com doença pulmonar obstrutiva crônica participar de estudos Fase I de terapia celular.
III. Excetuando-se as pesquisas envolvendo doenças crônicas os ensaios clínicos devem ser realizados somente se os benefícios previstos para cada sujeito de pesquisa e para a sociedade superarem claramente os riscos previstos.
IV. Em pacientes com doenças crônicas o tipo de pesquisa com desenho crossover pode ser útil para estudar a resposta de um paciente a curtos períodos de terapia, particularmente para condições crónicas nas quais a avaliação inicial da eficácia do tratamento se refere à medição do alívio de sintomas a curto prazo.
V. Ensaios clínicos randomizados controlados são mais úteis para o estudo de tratamentos para condições crônicas para os quais a terapia de manutenção é susceptível de ser continuado por longos períodos de tempo e se o efeito do tratamento ocorre logo após o início do tratamento e cessa logo após a retirada do tratamento.
O correto está em:
Sobre análise de sobrevida em ensaios clínicos em pacientes oncológicos.
I. Há dois tipos de estudos em oncologia que utilizam análise de sobrevida que podem utilizar o tempo como variável de interesse. Um deles é o estudo experimental (ensaios clínicos controlados aleatorizados), indicado para avaliar formas de tratamento.
II. Outro tipo de estudos em oncologia são os estudos de coorte observacionais, cujos dados podem ser obtidos pela coleta direta em prontuários médicos ou em bases de dados já existentes (dados secundários).
III. Essas fontes de dados secundários podem ser de base hospitalar (registros hospitalares de câncer) ou populacional (registros de câncer de base populacional).
IV. Na análise de sobrevida, os parâmetros mais importantes são a probabilidade de sobrevivência no curso de cada um dos intervalos considerados e a probabilidade de sobrevida acumulada (tratada correntemente como taxa de sobrevida), isto é, a probabilidade de sobreviver do tempo zero até o tempo final considerado.
V. Na análise de sobrevida pelo método de Kaplan-Meier os intervalos de tempo não são fixos, mas determinados pelo aparecimento de uma falha (por exemplo, o óbito). Nessa situação, o número de óbitos em cada intervalo deve ser um. Esse é um método não paramétrico, ou seja, que independe da distribuição de probabilidade
O correto está em:
Baseado na figura abaixo, escolha a alternativa que melhor responde a as informações farmacocinéticas de estudo de biodisponibilidade.
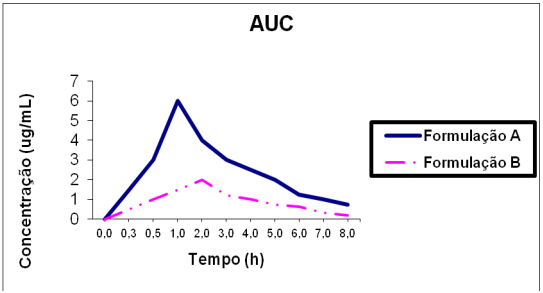
No que diz respeito aos aspectos éticos da pesquisa clínica envolvendo seres humanos, analise as afirmativas abaixo e marque a alternativa correta.
I. Quando houver necessidade de distribuição aleatória dos participantes da pesquisa em grupos experimentais e de controle, assegurar que, a priori, não seja possível estabelecer as vantagens de um procedimento sobre outro, mediante revisão de literatura, métodos observacionais ou métodos que não envolvam seres humanos.
II. Deve-se obter consentimento livre e esclarecido do participante da pesquisa e/ou seu representante legal, inclusive nos casos das pesquisas que, por sua natureza, impliquem justificadamente, em consentimento a posteriori.
III. Indivíduos ou grupos vulneráveis não devem ser participantes de pesquisa quando a informação desejada possa ser obtida por meio de participantes com plena autonomia, a menos que a investigação possa trazer benefícios aos indivíduos ou grupos vulneráveis.
IV. Deve-se assegurar aos participantes da pesquisa as condições de acompanhamento, tratamento, assistência integral e orientação, conforme o caso, enquanto necessário, inclusive nas pesquisas de rastreamento.
V. Deve-se utilizar o material biológico e os dados obtidos na pesquisa exclusivamente para a finalidade prevista no seu protocolo, ou conforme o consentimento dado pelo participante da pesquisa.
O correto está em: