O pH de um sistema tampão, constituído de um ácido fraco e...
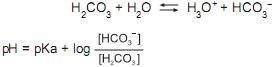
Sobre o equilíbrio de um sistema contendo 100 mL de solução 0,1 mol/L de H 2CO3 e 0,1 mol/L de HCO3– , quando se adiciona(m)
Comentários
Veja os comentários dos nossos alunos
Adicionando um ácido ou base forte, como as alternativas indicam, vai haver alguma alteração no pH mesmo que pequena. Exceto se a concentração for muuito baixa (cerca de 10^-8 mol/L).
No caso, a alternativa B é a correta. Adicionando NaOH, vamos ter mais OH- no meio reacional. Logo, se [H+].[OH-] = 1.10^-14, haverá uma diminuição na concentração de H+, o que desloca o equilíbrio para a direita (é como se retirássemos um pouco de H3O+).
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo