Dois tanques fechados de volumes V e 4V estão conectados por...
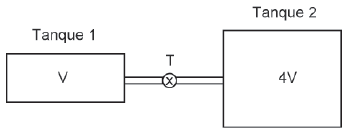
Inicialmente, o tanque 1 contém 1,40 mol de ar a 1,50 atm, o tanque 2 contém 0,700 mol de ar, e todo o sistema está em equilíbrio térmico com a vizinhança. Considere o ar um gás ideal. A válvula então é aberta. Após um tempo, o sistema atinge novamente a temperatura inicial.
Nessa situação final, a pressão no tanque 1, em atm, será, aproximadamente, de
Comentários
Veja os comentários dos nossos alunos
Antes de abrir a válvula.
P1*V1 = n*R*T1
P1*V1 / n = R*T
1,5*V / 1,4 = R*T
1,07*V = R*T
Após abrir a válvula.
Pf * Vf = n*R*T
Pf * 5V = n*1,07*V
Pf = 0,4494 atm
LETRA C
Fala galera, querem dicas de concursos da área técnica e um excelente material, sigam esse Instagram @ConcursosMinerva ou acessem o site: www.concursosminerva.com.br
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo