A reação de formação do KCI(s) e a variação da entalpia padr...
Próximas questões
Com base no mesmo assunto
Q398906
Química
A reação de formação do KCI(s) e a variação da entalpia padrão a ela associada estão representadas abaixo
K (s) + 1/2 Cl2(g)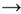 KCI(s)
KCI(s) 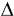 H = -424,2 kJ/mol
H = -424,2 kJ/mol
O ciclo de Born-Haber para essa reação é constituído por cinco etapas:
Etapa 1: conversão de K(s)em K(g) ;
Etapa 2: dissociação de 1/2 mol de Cl2(g) em átomos isolados de Cl(g).
Etapa 3: ionização de um mol de átomos de K(g) .
Etapa 4: adição de um mol de elétrons a um mol de átomos isolados de Cl(g).
Etapa 5: combinação de um mol de íons K+(g) e um mol de íons Cl-(g) dando origem à formação de um mol de KCI(s) .
Das etapas acima, são exotérmicas apenas:
K (s) + 1/2 Cl2(g)
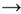 KCI(s)
KCI(s) 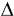 H = -424,2 kJ/mol
H = -424,2 kJ/molO ciclo de Born-Haber para essa reação é constituído por cinco etapas:
Etapa 1: conversão de K(s)em K(g) ;
Etapa 2: dissociação de 1/2 mol de Cl2(g) em átomos isolados de Cl(g).
Etapa 3: ionização de um mol de átomos de K(g) .
Etapa 4: adição de um mol de elétrons a um mol de átomos isolados de Cl(g).
Etapa 5: combinação de um mol de íons K+(g) e um mol de íons Cl-(g) dando origem à formação de um mol de KCI(s) .
Das etapas acima, são exotérmicas apenas: