Questões de Concurso Comentadas por alunos sobre transformações químicas em química
Foram encontradas 1.375 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. A Teoria Atômica de Dalton trouxe o átomo do campo filosófico para uma perspectiva científica. II. A descoberta dos raios catódicos foi fundamental para a conclusão de que a matéria é formada por partículas eletricamente carregadas. III. A estabilidade do modelo atômico de Rutherford poderia ser explicada pelas leis da Física Clássica, mas não pela Física de Planck-Einstein. IV. O efeito fotoelétrico observado por Einstein corroborou a idéia da dualidade onda-partícula dos elétrons.
Estão corretas apenas as afirmativas:
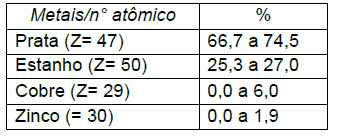
Roberto R. da Silva, et al. A química e a conservação dos dentes, Quím. Nov. na Esc.; N° 13, maio 2001.
Em relação aos metais presentes nas ligas e a tabela periódica é CORRETO a firmar:
Os diversos componentes presentes na água, que alteram seu grau de pureza, podem ser retratados em termos de suas características físicas, químicas e biológicas. Essas características podem ser traduzidas na forma de parâmetros de qualidade da água. Acerca desse assunto, julgue o item seguinte.
Alcalinidade é a concentração de cátions multimetálicos em
solução, como os divalentes Ca2+ e Mg2+.
A respeito dos conceitos relativos à química inorgânica, julgue o seguinte item.
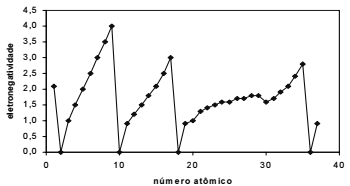
O gráfico abaixo permite concluir que a eletronegatividade é uma propriedade periódica.
I. Pela Lei de Boyel, um gráfico de volume versus pressão é uma parábola. II. O princípio de Avogadro pressupõe a existência de átomos e moléculas e principalmente, que no estado gasoso os átomos ou moléculas de um gás têm um tamanho muito pequeno quando comparados com o volume ocupado pelo conjunto de átomos ou moléculas do gás. Isso implica que o espaço vazio entre as moléculas gasosas deveria ser muito maior que as próprias moléculas. III. A pressão exercida por uma mistura de gases ideais é igual à soma das pressões parciais de cada gás da mistura. A pressão parcial de um gás ideal em uma mistura é definida como a pressão que ele exerceria se ocupasse sozinho o volume ocupado pela mistura na mesma temperatura da mistura.