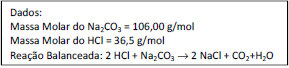Questões de Concurso
Para ufmt
Foram encontradas 9.522 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
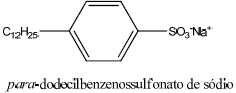
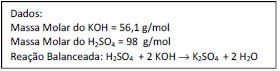
Assinale a sequência correta de reações que são realizadas no anel aromático do benzeno para obtenção dessa molécula.
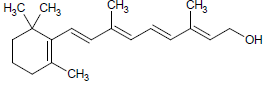 Assinale a alternativa que apresenta uma função orgânica presente na estrutura molecular plana da vitamina A.
Assinale a alternativa que apresenta uma função orgânica presente na estrutura molecular plana da vitamina A.

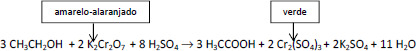
Verificando a intensidade de mudança de cor na solução por um sensor embutido no equipamento, pode-se estimar a quantidade de álcool presente no sangue do motorista. O limite atual é 0,05 miligramas por litro de ar expirado. Nesse caso, a variação no número de oxidação do átomo de cromo presente nos íons dessa reação é igual a:
2 H₂ + 2 NO → N₂ + 2 H₂O
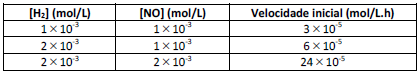
Marque a alternativa que apresenta a lei de velocidade que concorda com os dados experimentais.
( ) Quanto maior for a concentração dos reagentes, maior será a velocidade de reação. ( ) Colisões efetivas nem sempre levam à formação de novos produtos. ( ) Quanto maior a energia de ativação, mais rápida será a reação. ( ) Quanto maior a temperatura, maior será a velocidade de uma reação.
Assinale a sequência correta.

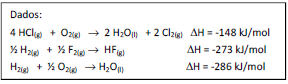
Dada a seguinte reação:
2 HCl(g) + F2(g) → 2 HF(g) + Cl2(g) ∆H = ?
Assinale a variação de entalpia, em kJ/mol, dessa reação.
I - Em uma cidade como Poços de Caldas, localizada a 1.196 metros acima do nível do mar, a temperatura de ebulição da água, em panela aberta, é superior a 100 °C como consequência da pressão atmosférica em Poços de Caldas ser maior que ao nível do mar. II - Na panela de pressão fechada, a água entra em ebulição acima de 100 °C graças à retenção de parte do vapor produzido, que gera aumento da pressão interna. III - Considerando três frascos iguais e fechados, numa mesma localidade, contendo volumes diferentes de água e todos mantidos à mesma temperatura, a pressão de vapor de água nos três frascos será a mesma em todos eles, desde que a quantidade de líquido colocada em cada um seja suficiente para que a quantidade de vapor formado atinja a pressão de vapor.
Está correto o que se afirma em