Questões de Concurso
Para ufmg
Foram encontradas 3.736 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
I. ( ) A educação superior tem por finalidade promover a produção e a difusão cultural do conhecimento desenvolvido pelo espírito científico e pelo pensamento reflexivo acadêmico a toda a sociedade. II. ( ) A educação superior tem por finalidade estimular o conhecimento dos problemas do mundo passado e presente, integrando conhecimentos que vão sendo adquiridos na estrutura sistematizadora do conhecimento. III. ( ) A educação superior tem por finalidade promover a divulgação de conhecimentos culturais, científicos e técnicos que constituem patrimônio da humanidade e comunicar o saber através do ensino, de publicações e de outras formas de comunicação. IV. ( ) A educação superior tem por finalidade promover a extensão, aberta à participação da comunidade acadêmica, visando à difusão das conquistas e benefícios resultantes da criação cultural e da pesquisa científica e tecnológica geradas na instituição. V. ( ) A educação superior tem por finalidade atuar em favor da universalização e do aprimoramento da educação básica, mediante a formação e a capacitação de profissionais, a realização de pesquisas pedagógicas e o desenvolvimento de atividades de extensão que aproximem os dois níveis escolares.
A sequência CORRETA é:
Assinale a alternativa CORRETA que completa o seguinte excerto do Artigo 214 da Constituição Federal de 1988:
A lei estabelecerá o plano nacional de educação, de duração decenal, com o objetivo de articular o sistema nacional de educação em regime de colaboração e definir diretrizes, objetivos, metas e estratégias de implementação para assegurar a manutenção e desenvolvimento do ensino em seus diversos níveis, etapas e modalidades por meio de ações integradas dos poderes públicos das diferentes esferas federativas que conduzam à
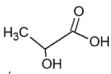
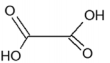
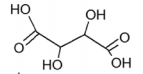
Ácido lático Ácido oxálico Ácido tartárico pKa = 3,85 pKa1= 1,25 ; pKa2 = 4,29 pKa1=3,04; pKa2=4,37
Em relação a esses ácidos, é CORRETO afirmar que
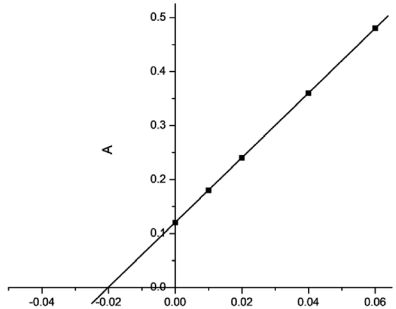 CPb adicionada (mg/L)
CPb adicionada (mg/L) Com base nos resultados, o teor de chumbo da amostra de tequila analisada é:
NaOH sólido; ácido acético (HAc) 2,00 mol L-1 (pKa = 4,74); ácido fosfórico (H3PO4) 2,00 mol L-1 (pKa1 = 2,23; pKa2 = 7,21; pKa3 = 12,32); amônia (NH3) 1,00 mol L-1 (pKa = 9,25); KH2PO4 sólido.
A mistura de quais dos reagentes acima, nas proporções adequadas, possibilita a preparação do tampão de pH 7,5, com boa capacidade de resistir às alterações de pH?
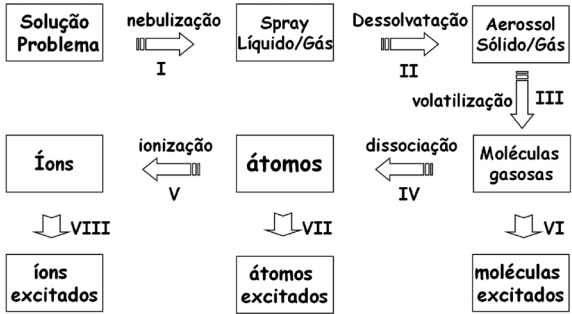
Considere o esquema e as seguintes afirmações:
I – A etapa IV é a responsável por produzir os átomos gasosos no estado fundamental. II – Na absorção atômica, utiliza-se um modulador, após a lâmpada, para eliminar os problemas que podem ser causados pela etapa VII. III – Somente a etapa V diminui a população de átomos gasosos no estado fundamental. IV – A etapa VII é indesejável para a absorção atômica, por diminuir a população de átomos gasosos no estado fundamental, porém é uma etapa essencial da espectrometria de emissão atômica.
Em relação a essas afirmativas, estão CORRETAS
I – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado, tanto por absorção de energia térmica da chama quanto da radiação de frequência característica proveniente da lâmpada de cátodo oco. II – Na absorção atômica, em chama, o analito deverá ser levado ao estado atômico gasoso. Após a atomização, o analito é levado ao estado excitado somente por absorção de energia térmica da chama, não sendo excitado pela radiação de frequência característica proveniente da lâmpada de cátodo oco. III – Agente liberador é a espécie introduzida para combinar-se com o componente da amostra que iria apresentar interferência devido à formação de compostos de baixa volatilidade (refratários) com o analito. IV – Agente liberador é a espécie introduzida para combinar-se com o analito, a fim de liberá-lo da interferência que sofreria devido à formação de compostos de baixa volatilidade (refratários).
Em relação a essas afirmativas, estão CORRETAS
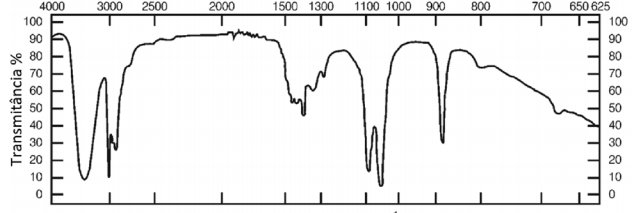 Número de onda (cm -1 ) De acordo com a análise do espectro, é CORRETO afirmar que o composto é
Número de onda (cm -1 ) De acordo com a análise do espectro, é CORRETO afirmar que o composto én-propanona 56,05 21,01 benzeno 80,09 2,28 n-propanol 97,20 20,80 isobutanol 107,89 17,93 n-butanol 117,73 17,84 n-pentanol 137,98 15,13
I – A ordem de eluição será de acordo com as temperaturas de ebulição, ou seja, n-propanona, benzeno, n-propanol, isobutanol, n-butanol e n-pentanol, que é diferente daquela que seria obtida com uma coluna apolar. II – Se, ao invés da temperatura constante fosse utilizada uma programação linear de temperatura, a ordem de eluição seria alterada. III – A constante dielétrica fornece uma medida aproximada da polaridade da molécula. IV – Se, ao invés da temperatura constante fosse utilizada uma programação linear de temperatura, o tempo de retenção seria certamente diferente dos obtidos no modo isotérmico.
De acordo com os dados fornecidos, estão INCORRETAS as informações
Acerca dessas semirreações, considere as afirmações a seguir:
I – A reação acontecerá de forma espontânea entre Fe3+ e MnO4 - na proporção estequiométrica de 5 para 1. II – O potencial padrão para a reação global será 2,28 V. III – Em uma titulação entre as duas espécies, o potencial do ponto de equivalência será apenas dependente dos potenciais padrão das semirreações e do pH do meio. IV – O íon permanganato é um agente redutor mais fraco que o íon hidrogênio.
Em relação a essas afirmativas, estão CORRETAS
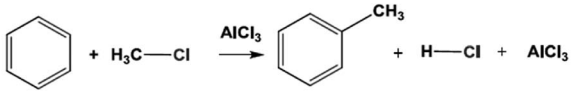
I – Nesta reação, o clorometano e o benzeno atuam como bases de Lewis. II – Neste processo, um par de elétrons π forma uma ligação química com o eletrófilo, promovendo a formação de uma carga positiva no interior do anel benzênico. III – Todas as etapas desta reação envolvem reações ácido-base. IV – O cloreto de alumínio tem basicamente duas funções: preparar o eletrófilo e recuperar a aromaticidade do anel.
Em relação a essas afirmativas, estão CORRETAS
Replicatas Estudante A Estudante B 1 32,35 31,0 2 33,60 31,5 3 34,55 32,0 4 31,05 31,5
Considerando os valores mostrados na tabela é CORRETO afirmar que
Abaixo está representado o ciclo de Born-Haber para o cloreto de sódio sólido.
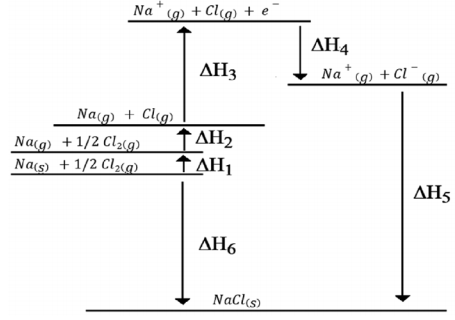
Qual das seguintes alternativas NÃO identifica corretamente a etapa correspondente na ilustração:

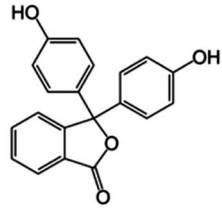
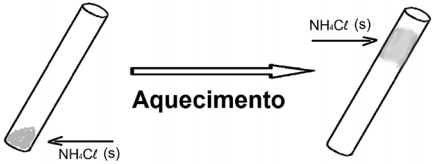
Com base nas observações do experimento, é CORRETO concluir que, nas condições em que o experimento foi realizado, o NH4 Cl