Questões de Concurso
Para professor - química
Foram encontradas 4.164 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Dentro desse contexto, leia com atenção as afirmações a seguir e marque V para as verdadeiras e F para as falsas.
( ) Rastreabilidade é a propriedade de o resultado de uma medição ou de o valor de um padrão estar relacionado a referências estabelecidas, geralmente a padrões nacionais ou internacionais.
( ) A incerteza de medição é um parâmetro associado ao resultado de uma medida que caracteriza a dispersão dos valores que podem ser, de um modo geral, atribuídos ao medidor.
( ) Seletividade de um método refere-se à extensão até a qual ele pode determinar analito(s) específico(s) em uma mistura complexa, sem interferência dos outros componentes na mistura.
( ) Para a análise quantitativa, a faixa de trabalho para um método é determinada pelo número de amostras com concentrações iguais de analito, de tal forma que a incerteza alcançada possa ser admissível.
( ) A validação de um método é necessária para demonstrar que ele é cientificamente coerente, sob as condições nas quais ele deve ser aplicado.
Escolha e assinale a opção que contenha a sequência CORRETA de cima para baixo.
Associe a coluna da direita com a da esquerda de acordo com as características de cada tipo de reação.
(1) Substituição em alcanos.
(2) Adição em alcenos.
(3) Reação de eliminação.
(4) Reação de oxidação.
( ) É utilizada para transformar óleos vegetais em gorduras, como margarina.
( ) É utilizada para obtenção de haletos orgânicos saturados.
( ) Formação de ácido etanoico a partir do but-2-eno.
( ) Reação entre etanol e metilpropan-2-ol, produzindo éter etil-t-butílico.
A ordem CORRETA de associação, de cima para baixo, é:

Nesse experimento, abordam-se vários assuntos da Química e dos Processos Químicos. Assinale a alternativa que NÃO associa de forma correta esses procedimentos com o assunto a ser estudado.
( ) Os protozoários são microrganismos eucarióticos unicelulares que ingerem partículas alimentares, não apresentam parede celular rígida e nem clorofila. Alguns movem-se na água por apêndices chamados cílios ou flagelos.
( ) As algas são consideradas semelhantes às plantas porque contêm o pigmento verde clorofila, mas diferentemente das plantas, as algas não apresentam uma parede celular rígida. Esses eucariotos podem ser unicelulares e microscópicos, ou multicelulares. Podem causar problemas ambientais pela liberação de substâncias químicas tóxicas.
( ) Os fungos são microrganismos procariotos que têm parede celular e podem ser uni ou multicelular. Alguns fungos são cultivados em madeira úmida ou solo e são utilizados como alimentos humanos. As leveduras são fungos unicelulares benéficos, amplamente utilizadas na produção de bebidas alcoólicas fermentadas que não causam dano à saúde humana.
( ) As bactérias são seres procariotos sem membrana nuclear, subdivididas em dois grupos: as eubactérias e as arqueobactérias. As primeiras apresentam formas variadas, especialmente esféricas, bastonetes e espirilos. Muitas arqueobactérias possuem habilidade em sobreviver em ambientes não-usuais, como aqueles com altas concentrações salinas ou elevada acidez e altas temperaturas.
Assinale a alternativa que contém a sequência CORRETA de cima para baixo.
Fonte: Campbell, Mary K.; Farrel, Shawn O. Bioquímica: combo. 5a Ed. Cengage Learning. São Paulo, 2011.
Qual alternativa abaixo contém a explicação CORRETA sobre a conformação tridimensional das proteínas? Assinale-a.
( ) A remoção de sólidos grosseiros, deve ser aplicada a qualquer água residuária e pode consistir de peneiras ou caixas separadoras.
( ) Para a remoção de materiais flotáveis, utiliza-se, por exemplo, grades de separação.
( ) Para a depuração de águas residuárias de processos biológicos, pode-se utilizar o lodo ativado.
( ) Para a remoção de nutrientes nos efluentes, o carvão ativado não é uma possibilidade, pois sua eficiência é para a retirada de gases dissolvidos.
Assinale a alternativa que contém a sequência CORRETA, de cima para baixo.
As alternativas abaixo apresentam esses princípios, EXCETO uma, assinale-a.
( ) As pilhas que não podem ser recarregadas são classificadas como sistemas eletroquímicos primários ou baterias primárias.
( ) O destino ideal de pilhas e baterias usadas deveria ser o aterro controlado, pois todo o lixo recebe uma cobertura de PVC ou argila, o que evita contaminação do ambiente.
( ) As baterias de níquel/cádmio são baterias secundárias e de longa duração.
( ) Na pilha alcalina não há formação de gás hidrogênio, pois o meio é básico.
( ) Nas pilhas de mercúrio, usadas em relógios e calculadoras, o mercúrio é oxidado a óxido de mercúrio, que é solúvel e pode contaminar o solo se descartada incorretamente.
Assinale a opção que contenha a sequência CORRETA de cima para baixo.
Assinale a alternativa CORRETA, sobre os objetivos e as modificações introduzidas pela 17025.
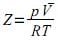
A respeito dos gases ideais e reais, assinale a alternativa CORRETA.
“A maior parte [da água da Terra] veio dos asteroides que deram uma contribuição de mais de 50%. Uma pequena parcela veio da nebulosa solar, com 20% de participação e os 30% restantes, dos cometas.”
(Fonte: http://www.inovacaotecnologica.com.br/noticias/noticia.php?artigo=origem-da-agua-da-terra#.VAOaaPldVqU. Acessado em 31/08/2014.)
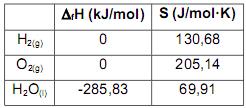
Considerando-se a reação de formação da água líquida a partir de seus elementos, ocorrendo a 25ºC, em condições de temperatura e pressão constantes, e os valores termodinâmicos apresentados a seguir, assinale a alternativa CORRETA.
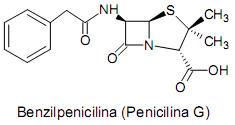
As amidas podem ser preparadas pela reação de um cloreto de ácido com uma amina, então, na intensão de produzir um repelente de insetos muito utilizado pela indústria cosmética conhecido como DEET, com nomenclatura IUPAC de N,N-dietil-3-metilbenzamida, assinale a alternativa CORRETA que indica quais reagentes um químico deve procurar em seu almoxarifado:
lEm 1913, há mais de 100 anos, Alfred Werner foi honrado com o Prêmio Nobel de Química por seu brilhante trabalho sobre a ligação existente em complexos de coordenação. No final do século XIX, ele concluiu que nos complexos o metal possui dois tipos de valência: a primária (que hoje entendemos como a carga iônica do complexo formado) e a secundária (que corresponde ao número de ligantes coordenados com o íon central). Atualmente as ligações nos compostos de coordenação são explicadas pelas Teorias da Ligação de Valência (TLV), do Campo Cristalino (TCC) e do Orbital Molecular (TOM), porém, a Teoria de Werner ainda hoje continua útil para estudos sobre algumas propriedades dos compostos de coordenação, como a estereoquímica.
Em uma aula prática de química, os estudantes formaram alguns complexos em solução. Com o objetivo de estimular os alunos a buscarem informações extras sobre o assunto tratado em aula, o professor exigiu uma pesquisa sobre os compostos.
Observe os compostos formados, considere sua conformação tridimensional e associe a coluna da direita com a da esquerda.
(1) [Pt(NH3)2CI2]
(2) [Pt(NH3)4Cl2] 2+
(3) [Co(NH3)5Cl] 2+
(4) [Pt(NH3)3Cl3] +
( ) A valência primária é 2 e a secundária é 6; não apresenta isômeros.
( ) A carga do metal é 2+ e apresenta isomeria óptica
( ) Possui dois isômeros Fac (facial) e Mer (meridional).
( ) Possui conformação octaédrica com dois isômeros Cis e Trans.
Assinale a alternativa que apresenta a ordem CORRETA de associação, de cima para baixo.
Considerando as alterações morfológicas e bioquímicas desse processo, assinale a alternativa na qual NÃO se encontram as características desse fenômeno.
( ) A conformação de menor tensão estérica para o composto cis-1-tert-butil-4- bromocicloexano é a conformação onde o grupo tert-butila é equatorial e o bromo, axial.
( ) Considerando que a interação gauche entre os grupamentos metila gera uma tensão estérica de 3,8 KJ/mol e as interações axiais CH3 ? H geram tensão estérica de mesmo valor (3,8 KJ/mol), pode-se dizer que para o composto trans-,2-dimetilcicloexano não há diferença de energia entre a conformação da molécula que mantém os grupos metila em posições axiais e a conformação que as mantém em posições equatoriais.
( ) Na conformação de compostos cis-1,3-dissubstituídos, só é possível os substituintes de uma mesma molécula permanecerem ao mesmo tempo em posição axial ou equatorial, enquanto nos compostos trans-1,3-dissubstituídos, os substituintes de uma mesma molécula, ao contrário, não permanecerão ao mesmo tempo em posição axial ou equatorial.
( ) O substituinte tert-butil causa maior tensão 1,3-diaxial em um cicloexano monossubstituído que o isopropil.
Assinale a alternativa que contém a sequência CORRETA de cima para baixo.
Dentro desse contexto, leia com atenção as afirmações a seguir e marque V para as verdadeiras e F para as falsas:
( ) Na análise titrimétrica, trata-se a substância a ser determinada com um reagente adequado, na forma padronizada, e determina-se o volume necessário para completar a reação.
( ) A análise térmica diferencial registra a diferença de temperatura de uma substância, antes e depois de reagir com um material de referência.
( ) Na espectroscopia de absorção atômica, o material a ser analisado é vaporizado sob vácuo e o vapor é submetido a um feixe de elétrons de alta energia.
( ) Os métodos espectrométricos de análise dependem da medida da quantidade de energia radiante, com um determinado comprimento de onda, que é absorvida ou emitida pela amostra.
( ) Os métodos de emissão submetem a amostra a um tratamento térmico ou elétrico que leva os átomos a estados excitados que emitem energia. A intensidade dessa energia é, então, medida. São exemplos dessa técnica, a fotometria de chama e a fluorimetria.
Assinale a alternativa que contém a sequência CORRETA de cima para baixo.
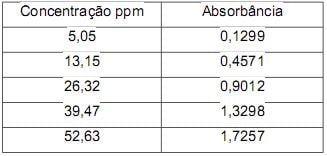
Com esses dados, os alunos fizeram a regressão linear, obtendo a equação da reta (y = a.x + b), com os seguintes valores: R2 = 0,9979; a = 0,0333; b = - 0,0023.
Com base nesse experimento, julgue (V) verdadeiro ou (F) falso os itens a seguir.
( ) A concentração de flavonoides no suco de uva da cantina será de 25 ppm de a absorbância apresentada em 510 nm for de 0,8302.
( ) A concentração de flavonoides no suco de uva será de 0,01% se a absorbância for de 0,3307.
( ) O valor da absorbância dos flavonoides do suco de uva não vai ser alterado em função do caminho óptico.
( ) A temperatura e o tipo de solvente são fatores que não influenciam as absortividades molares das substâncias.
Assinale a alternativa que apresenta a sequência CORRETA de cima para baixo.
Ka do ácido fórmico (HCOOH) = 0,00018
pKa do ácido benzóico (C6H5COOH) = 4,20
Analise as asserções a seguir.
Tanto o ácido fórmico quanto o ácido benzóico são considerados ácidos fracos, porém o ácido fórmico é um ácido mais fraco que o ácido benzóico
PORQUE
o ácido benzóico estabiliza bem a carga iônica por ressonância no anel aromático, ionizando- se em maior proporção que o ácido fórmico quando em solução aquosa.
Assinale a alternativa CORRETA.
NH4NO3 ? 2N2 + 4H2O + O2
O nitrato de amônio é produzido pela simples neutralização do ácido nítrico, pelo amoníaco segundo a reação:
NH3(g) + HNO3(aq) ? NH4NO3(aq)
Em um estudo sobre a cinética dessa reação foram obtidos os seguintes dados:
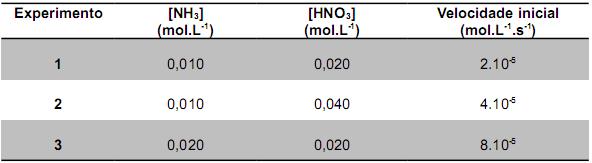
Como base nesses dados cinéticos e na estequiometria da reação, assinale a alternativa CORRETA.