Questões de Vestibular Comentadas sobre química
Foram encontradas 1.418 questões
Considere o seguinte composto.
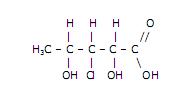
Assinale a alternativa que contém, respectivamente, o número de diferentes isômeros ópticos e o de misturas racêmicas do composto anterior.
NaCl + MnO2 + H2SO4 → Na2SO4 + Cl2 + H2O
Sabendo que a mesma teve um rendimento de 80% e foi realizada a uma temperatura de 27 °C e a uma pressão de 1 atm e que utilizou 600 g de NaCl, o volume de Cl2 obtido, em litros, foi, aproximadamente,
A água não deve ser usada para apagar certos tipos de incêndios, porque a molécula de H2O, quando exposta a altas temperaturas, decompõe-se em gás hidrogênio, um explosivo, e em gás oxigênio, que aumenta a chama, por ser comburente.
Se o bicarbonato de sódio (NaH2CO3), principal constituinte de alguns tipos de extintores de incêndio, for obtido a partir da reação exotérmica de neutralização, conforme equilíbrio químico representado pela equação H2CO3(aq) + NaOH(aq)
 NaHCO3(aq) + H2O(l)
NaHCO3(aq) + H2O(l)então o rendimento da reação seria maior se a temperatura aumentasse e o pH diminuísse.
Os açúcares são solúveis em água e se oxidam devido, respectivamente, à presença, em suas moléculas dos grupos funcionais
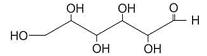
A quantidade de carbonos quirais na molécula de glicose mostrada na figura acima é igual a
No processo de oxidação da glicose, são rompidas ligações iônicas, para a formação de ligações covalentes, mais estáveis.
Se, em repouso, uma pessoa consome 0,34 L de oxigênio por minuto, então o aumento da temperatura do ar resultará em massa menor de oxigênio consumido por minuto pela pessoa, o que explica o fato de ser mais difícil se respirar em dias muito quentes.
A reação de combustão da glicose, por ser endotérmica, é um processo espontâneo.
Dado que glicose e sacarose (C12H22O11) são solutos não eletrólitos e não voláteis, iguais quantidades, em mol, dissolvidos em mesma quantidade de água causam, qualitativamente e quantitativamente, os mesmos efeitos tonoscópicos e ebulioscópicos nessas soluções.
Na tabela a seguir, são apresentadas informações contidas na bula de comprimidos sólidos de ibuprofeno.
cada comprimido contém
ibuprofeno____|___ 300 mg
excipientes ___|___ ácido cítrico, benzoato de sódio,dióxido de titânio e amido
Assinale a opção que apresenta o gráfico que melhor representa a variação da temperatura em função do tempo para um comprimido que tenha a composição mostrada na tabela e tenha sido macerado e aquecido.
A massa molar da fórmula molecular mínima do ibuprofeno é 220,0 g/mol.
A presença dos anéis benzênicos na estrutura do benoxaprofeno faz que essa molécula seja plana.
A substituição do grupo — CH3 na estrutura do benoxaprofeno por um — Cl gera um ácido mais forte que o benoxaprofeno.


