Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
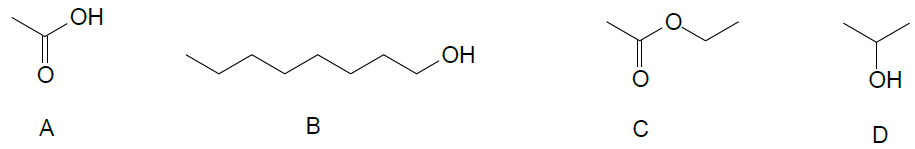
Dentre essas moléculas, as que apresentam baixa solubilidade em água são os compostos
Dados: R = 0,08 L.atm.K-1 .mol-1 MM(CO2) = 44 g.mol-1
Com o aumento da temperatura, a pressão do sistema, em atm, sofrerá um aumento de quantas unidades?
Dados: MM(H) = 1 g.mol-1 , MM(C) = 12 g.mol-1 e MM(O) = 16 g.mol-1
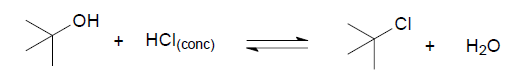
Considerando-se as características dos reagentes envolvidos na reação, constata-se que o processo de formação do cloreto de t-butila envolve
A unidade de repetição do polímero que representa o náilon é a:
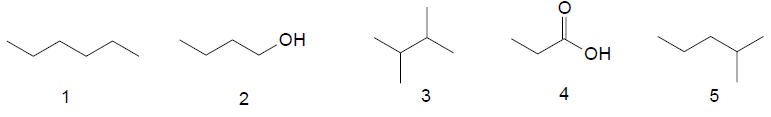
Qual desses compostos orgânicos apresenta a menor temperatura de ebulição?
PCl3 BF3 SO2 SO4 2- NH4 + 1 2 3 4 5
Qual molécula ou íon apresenta geometria molecular angular?
A + B ⇌ C + D
O valor numérico da constante de equilíbrio, Kc, será igual a:
O álcool etílico combustível, mais popularmente conhecido como etanol, é uma fonte de energia limpa e renovável, proveniente de várias matérias-primas como beterraba, milho e cana-de-açúcar, sendo esta última o insumo agrícola mais utilizado na produção de etanol no Brasil.
Ao contrário dos combustíveis fósseis, o etanol é uma fonte de energia natural e limpa, pois sua composição não contém poluentes que sejam prejudiciais à saúde e ao meio ambiente. Desde o momento em que brota no campo, a cana-de-açúcar passa a absorver parte do gás carbônico utilizado na produção e no consumo do etanol.
A crescente fabricação brasileira de carros flex (movidos a gasolina e etanol), iniciada em 2003, foi o que permitiu o avanço da utilização do etanol no Brasil. Atualmente, 97,7% dos carros produzidos no país podem ser abastecidos com etanol ou gasolina, puros ou misturados em qualquer proporção.
A equação química que representa o processo de combustão do etanol encontra-se mostrada a seguir.
C2H6O(l) + 3O2(g) → 2CO2(g) + 3H2O(l)
Sabendo-se que a entalpia de formação da H2O(l) é -286 kJ/mol; que a do CO2(g) é - 393,5 kJ/mol e que a do C2H6O(l) é - 277,6 kJ/mol, verifica-se que a energia liberada na combustão de 1,0 mol de etanol é:
Isômeros são compostos com a mesma composição química, mas diferentes estruturas. Essas diferenças provocam alterações significativas nas propriedades químicas e físicas desses compostos. As figuras a seguir representam três isômeros do pentano (C5H12).
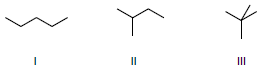
Sabendo-se que a temperatura de ebulição depende da intensidade das forças intermoleculares, a qual depende da geometria molecular, a ordem crescente de temperatura de ebulição dos três isômeros do pentano apresentados é, respectivamente:
Uma pilha de Daniel é um dispositivo capaz de transformar energia química em energia elétrica, e como exemplo
tem-se uma formada por eletrodos de ferro 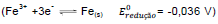 e estanho
e estanho 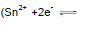
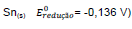 . Nesse caso, constata-se que
. Nesse caso, constata-se que
Questão 38 As chalconas são uma classe de moléculas que possuem vários tipos de atividades farmacológicas. No processo de cristalização de um dos derivados de chalcona, mediu-se uma variação da energia livre de Gibbs e da entalpia a 27 °C de -64 kcal.mol-1 e -164 kcal.mol-1 , respectivamente.
Nesse caso, a temperatura, em Kelvin, a partir da qual a cristalização sofrerá uma transição de um processo espontâneo para não-espontâneo, será de aproximadamente
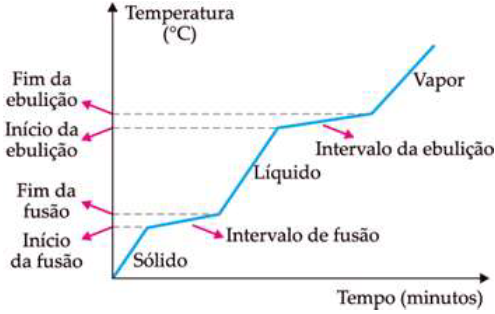
O gráfico indica a mudança de estado físico, por alteração na temperatura, de uma liga metálica de ouro/cobre. A análise gráfica permite concluir que
