Questões de Vestibular Sobre química
Foram encontradas 6.520 questões
A região da molécula enzimática, na qual ocorre a ligação ao substrato, é denominada sítio ou centro ativo e tem especificidade pelo substrato, a ponto de diferenciar moléculas muito semelhantes, como os anômeros α e β da D-Glicose.
Quando os aminoácidos glicina (pKαCOOH =2,34; pKαNH2 =9,60) e histidina (pKαCOOH =1,82; pKαNH2 =9,17; pKR =6,0) são submetidos a eletroforese em pH=7,6, o primeiro migrará para o polo negativo e o último migrará para o polo positivo.
O ácido aspártico, contendo cinco átomos de carbono na cadeia principal, é um aminoácido que recebe essa denominação por apresentar um caráter ácido em pH=7,0 devido à presença de um grupamento carboxila extra ligado ao átomo de carbono α da molécula.
Os aminoácidos, quando dissolvidos em solução aquosa, dependendo do pH dessa solução, podem ter carga líquida positiva, negativa ou nula, sendo essa propriedade utilizada para separá-los por eletroforese.
O aminoácido arginina pertence ao grupo cujas cadeias laterais são ácidas em pH=7,0 devido à presença de mais um grupo carboxílico na molécula, além daquele ligado ao carbono α.
Água do mar = 32 mL Água purificada = 68 mL
Considerando que a água do mar contém salinidade média de 3,5% (m/V) e que sua densidade é de 1,0 g.mL−1, a salinidade da solução para lavagem nasal, em porcentagem (m/V), é, aproximadamente, igual a
De acordo com o texto, para cada hectare de vegetação em fase de crescimento, o volume máximo de CO2, nas CATP, que pode ser retirado da atmosfera, em m3, corresponde a, aproximadamente, Dados: Volume molar de qualquer gás, nas CATP = 25 L . mol-1 Massa molar do CO2 = 44 g . mol−1
(Adaptado Revista Scientific American Brasil, agosto de 2013. p. 13)
A porcentagem, em massa de silício, na sílica é de:
Dado: Massas molares (g . mol−1):
O = 16 Si = 60
(Adaptado Revista Scientific American Brasil, agosto de 2013. p. 13)
Os isótopos oxigênio−18 e oxigênio−16 possuem, necessariamente,
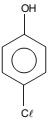
Massa molar = 128,5 g/mol
O número de moléculas existente em 0,257 mg desse corante é: Dado: Constante de Avogadro = 6,0 × 1023 mol−1

Massa molar = 128,5 g/mol
Esse composto
I. possui anel aromático.
II. apresenta a função fenol.
III. forma ligações de hidrogênio com a água.
Está correto o que se afirma em
(Adaptado: Revista Mundo Estranho, setembro de 2013. p. 49)
Para elevar o pH da água da chuva, pode-se adicionar a substância
(Adaptado: Revista Mundo Estranho, setembro de 2013. p. 49)
O índice normal da água, ou seja, pH = 7, a 25 °C, corresponde à concentração de íons OH− igual a
Dado: Kw, a 25 °C = 1,0 × 10−14
Dados: Densidade do PET = 1,3 g cm-3 . Considere que no reaproveitamento do PET não ocorre perda de massa, e que o volume externo da garrafa é de 600 mL.
O nome da Propionibacterium acnes vem da sua capacidade de produzir um ácido carboxílico, o ácido propanoico (também chamado de propiônico), como subproduto de seu metabolismo. Não se conhece o papel desse ácido, se houver, na patologia da acne.
Suponha que um adolescente que sofre de acne resolve passar etanol no rosto e que esse álcool reagirá com o ácido propanoico produzido pelas bactérias. Sobre essa reação de condensação, considere as afirmativas abaixo.
I – Um dos produtos da reação terá uma ligação éster
II – Na reação haverá formação de água.
III – O produto maior terá cinco carbonos.
IV – A reação formará propanoato de etila.
Está correto o que se afirma em: