Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
No ano de 2014, o Estado de São Paulo vive uma das maiores crises hídricas de sua história. A fim de elevar o nível de água de seus reservatórios, a Companhia de Saneamento Básico do Estado de São Paulo (Sabesp) contratou a empresa ModClima para promover a indução de chuvas artificiais. A técnica de indução adotada, chamada de bombardeamento de nuvens ou semeadura ou, ainda, nucleação artificial, consiste no lançamento em nuvens de substâncias aglutinadoras que ajudam a formar gotas de água.
(http://exame.abril.com.br. Adaptado.)
Uma das substâncias aglutinadoras que pode ser utilizada para a nucleação artificial de nuvens é o sal iodeto de prata, de fórmula AgI. Utilizando os dados fornecidos na Classificação Periódica dos Elementos, é correto afirmar que o cátion e o ânion do iodeto de prata possuem, respectivamente,
Dados de massas molares em g mol-1 : C=12; N=14 e O=16.
CH3OH(g)+ 3/2 O2(g) → CO2(g) + 2 H2O(g) combustão direta
CH3OH(g)+H2O(g) → CO2(g) + 3H2(g) H2(g)+ ½ O2(g) → H2O(g) geração e queima de hidrogênio
De acordo com essas equações, o processo de geração e queima de hidrogênio apresentaria uma variação de energia
Dados: Equação da reação: ½ N2 + O2 → NO2
Massas molares em g mol-1: N2=28 , O2=32 e NO2= 46
NH4NO3(s)+H2O( l ) →NH4+(aq)+NO3-(aq) ΔΗ = 26 kJ mol-1 1
CaCl2(s)+H2O( l ) →Ca2+ (aq)+2Cl-(aq) ΔΗ = - 82 kJ mol-1 2
De acordo com a notação química, pode-se afirmar que as equações 1 e 2 representam processos de
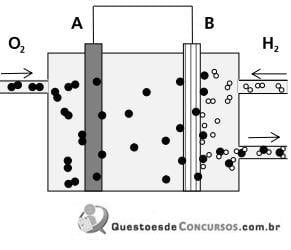
Nesse esquema, os círculos podem representar átomos, moléculas ou íons. De acordo com essas informações e o conhecimento de eletroquímica, pode-se afirmar que nesse dispositivo a corrente elétrica flui de
C3H8 + 5O2 ? 3CO2 + 4H2O
Admitindo que 30 L, medidos em CNTP (273,15 K e 1 atm), tenham sido queimados na presença de um determinado volume de ar cuja porcentagem de oxigênio é igual a 20% do volume, também medidos em CNTP, assinale o volume de ar necessário para promover a combustão completa do propano.
BaCl2 (s) + Na2 SO4 (aq) → BaSO4 (s) + 2NaCl(aq)
Massas Molares (g.mol -1 )
BaCl2= 208
Na2SO4 = 142
BaSO4 = 233
NaCl = 58,5
Se 5,2 g de BaCl2 são misturados com 5,0 g de Na2SO4, a massa aproximada de BaSO4 obtida, em gramas, será de
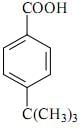
O número máximo de compostos que poderia corresponder ao composto orgânico em questão é igual a
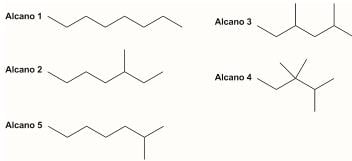
Dentre os compostos apresentados, o que apresenta a menor temperatura de ebulição é o