Questões de Vestibular Sobre química
Foram encontradas 6.605 questões
Dados: Densidade do PET = 1,3 g cm-3 . Considere que no reaproveitamento do PET não ocorre perda de massa, e que o volume externo da garrafa é de 600 mL.
Considerando que 96.500 C é a quantidade de carga transportada por 1mol de elétrons, é CORRETO afirmar que a fórmula do composto de brometo é
Sobre os compostos de cálcio, assinale a afirmativa INCORRETA.
Sobre a reatividade dos alquenos, assinale com V para as alternativas verdadeiras e com F para as falsas.
( ) O mecanismo de adição aos alquenos é o ataque nucleofílico aos hidrogênios de uma ligação dupla.
( ) A reação de bromação do alqueno é caracterizada pela mudança de cor na solução de bromo à medida que o bromo reage com o alqueno.
( ) Os átomos de carbono da ligação dupla tem hibridização sp2 e usam três orbitais híbridos para formar três ligações sigma.
( ) A desidro-halogenação é caracterizado pela remoção de dois átomos de halogênios de átomos de carbonos vizinhos.
A sequência CORRETA é
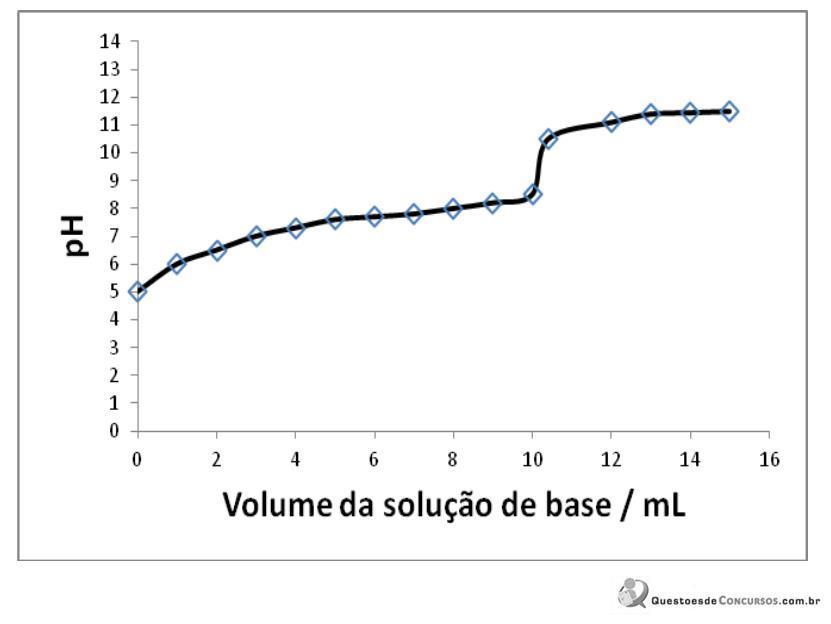
Sobre essa titulação foram feitas as seguintes afirmações:
I. a concentração inicial do ácido é 10-5 mol/L.
II. o ácido envolvido na titulação é fraco.
III. o reagente titulante é uma base forte.
A partir dessa análise, conclui-se que estão CORRETAS as afirmativas
C8H18 (L) + 25/2 O2(g) ➡ 8CO2(g) + 9H2O(L) Δ H0 = -5471KJ
Nestas condições, é CORRETO afirmar que a razão entre as energias gastas em um ano, nessa jornada, pelo automóvel e o estudante na bicicleta, é aproximadamente
Sobre a molécula 2- buteno foram feitas as seguintes afirmações:
I. os carbonos da ligação dupla da molécula 2- buteno têm cada um, um orbital p não hibridizado.
II. as ligações duplas entre carbonos são de difícil rotação devido as ligações sigma que se superpões lateralmente.
III. a densidade eletrônica na ligação π está acima e abaixo dos eixos de ligação, enquanto nas ligações σ a densidade eletrônica localiza-se ao longo do eixo de ligação.
A partir dessa análise, conclui-se que estão CORRETAS as afirmativas
Sobre os números quânticos propostos no modelo de Bohr e no modelo da mecânica quântica, é CORRETO afirmar que
Nessas condições, é CORRETO afirmar que o volume necessário da solução estoque para você preparar 500mL de uma solução de HCl 0,5mol/L é igual a
O nome da Propionibacterium acnes vem da sua capacidade de produzir um ácido carboxílico, o ácido propanoico (também chamado de propiônico), como subproduto de seu metabolismo. Não se conhece o papel desse ácido, se houver, na patologia da acne.
Suponha que um adolescente que sofre de acne resolve passar etanol no rosto e que esse álcool reagirá com o ácido propanoico produzido pelas bactérias. Sobre essa reação de condensação, considere as afirmativas abaixo.
I – Um dos produtos da reação terá uma ligação éster
II – Na reação haverá formação de água.
III – O produto maior terá cinco carbonos.
IV – A reação formará propanoato de etila.
Está correto o que se afirma em:

I - Para Lewis, uma base caracteriza-se por ser capaz de receber um par de elétrons.
II - Segundo a de? nição de base por Brønsted-Lowry, o propranolol comporta-se como base por receber um H+.
III - No conceito de Arrhenius, um ácido é aquela substância que libera íons H+ em solução aquosa.
É correto APENAS o que se afirma em:

O(s) produto(s) da reação de decomposição térmica do carbonato de cálcio é(são).
Sabendo-se que a fórmula do cloreto de ouro é AuCl3 ou Au2 Cl6 , conclui-se que o número de oxidação do ouro nessa molécula é
Em escritos anteriores ao século XVI, há referência apenas a cenouras de cor roxa, amarela ou vermelha. É possível que as cenouras de cor laranja sejam originárias dos Países Baixos, e que tenham sido desenvolvidas, inicialmente, à época do Príncipe de Orange (1533-1584).
No Brasil, são comuns apenas as cenouras laranja, cuja cor se deve à presença do pigmento betacaroteno, representado a seguir.
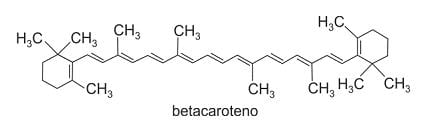
Com base no descrito acima, e considerando corretas as hipóteses ali aventadas, é possível afirmar que as cenouras de coloração laranja
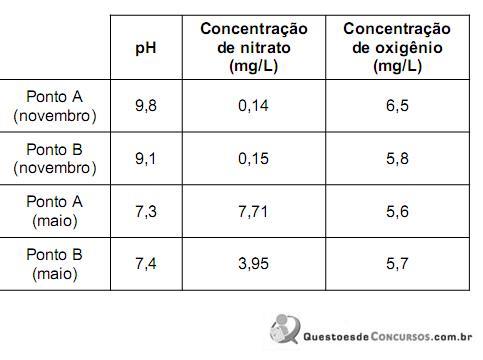
Com base nas informações da tabela e em seus próprios conhecimentos sobre o processo de fotossíntese, um pesquisador registrou três conclusões:
I. Nessas amostras, existe uma forte correlação entre as concentrações de nitrato e de oxigênio dissolvidos na água.
II. As amostras de água coletadas em novembro devem ter menos CO2 dissolvido do que aquelas coletadas em maio.
III. Se as coletas tivessem sido feitas à noite, o pH das quatro amostras de água seria mais baixo do que o observado.
É correto o que o pesquisador concluiu em
Dados: Massas molares (g/mol) H = 1,00 O = 16,0 Cu = 63,5
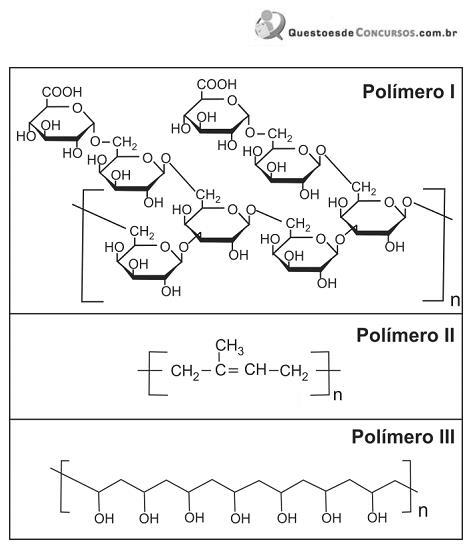
Para remover os resíduos de polímero das peças, o funcionário dispunha de apenas dois solventes: água e n-hexano. O funcionário analisou as fórmulas estruturais dos três polímeros e procurou fazer a correspondência entre cada polímero e o solvente mais adequado para solubilizá-lo. A alternativa que representa corretamente essa correspondência é: