Questões de Vestibular
Sobre radioatividade: reações de fissão e fusão nuclear, desintegração radioativa e radioisótopos. em química
Foram encontradas 176 questões
Um sistema contém 124 g de um radioisótopo hipotético abX cujo tempo de meia-vida é de 8 anos e que se transforma no elemento químico a-20b-8Y após o decaimento radioativo. O tempo, em anos, necessário para que a massa do radioisótopo seja reduzida a 25 % da massa inicial, e o número de partículas β emitidas no processo
No dia 11 de fevereiro, comemora-se o Dia Internacional das Mulheres e Meninas na
Ciência, data estabelecida pela Assembleia Geral da ONU em reconhecimento ao trabalho feminino
para o desenvolvimento científico. Dentre tantas mulheres que contribuíram para a ciência no século
XX, a física nuclear austríaca Lise Meitner (1878-1968) se destacou por suas descobertas e pela
Teoria da Fissão Nuclear, sendo, inclusive, considerada a mãe da era atômica.
 https://www.thefamouspeople.com/profiles/images/lise-meitner-3.jpg. Acesso em 02.fev.2019.
https://www.thefamouspeople.com/profiles/images/lise-meitner-3.jpg. Acesso em 02.fev.2019. A teoria que deu o título de mãe da era atômica à Lise Meitner consiste no
Algumas categorias de câncer de tireoide podem ser tratadas por meio de um tipo de radioterapia em que o radioisótopo é disponibilizado no interior do organismo do paciente. Dessa forma, a radiação é emitida diretamente no órgão a ser tratado e os efeitos colaterais são diminuídos. O radioisótopo usado nesse tipo de radioterapia decai de acordo com a equação.
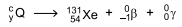
O radioisótopo 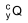 é inserido em cápsulas. Para realizar a
radioterapia, o paciente é isolado em instalação hospitalar
adequada onde ingere uma dessas cápsulas e permanece
internado até que a atividade do radioisótopo atinja valores
considerados seguros, o que ocorre após o tempo mínimo
correspondente a 3 meias-vidas do radioisótopo.
é inserido em cápsulas. Para realizar a
radioterapia, o paciente é isolado em instalação hospitalar
adequada onde ingere uma dessas cápsulas e permanece
internado até que a atividade do radioisótopo atinja valores
considerados seguros, o que ocorre após o tempo mínimo
correspondente a 3 meias-vidas do radioisótopo.
A figura apresenta a curva de decaimento radioativo para 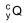 .
.
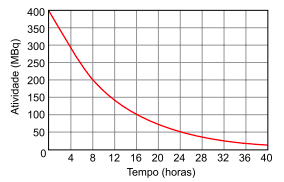
(http://www.scielo.br/pdf/abem/v51n7/a02v51n7.pdf. Adaptado)
O radioisótopo 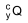 e o tempo mínimo que o paciente deve
permanecer internado e isolado quando é submetido a esse
tipo de radioterapia são, respectivamente,
e o tempo mínimo que o paciente deve
permanecer internado e isolado quando é submetido a esse
tipo de radioterapia são, respectivamente,
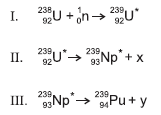
Considerando-se as informações do texto, as equações nucleares, com base na tabela periódica e nas tendências das propriedades dos elementos químicos, é correto afirmar:
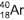 , originário do decaimento radioativo do potássio 40,
, originário do decaimento radioativo do potássio 40,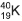 , e o xenônio tem nove, a exemplo do
xenônio 129,
, e o xenônio tem nove, a exemplo do
xenônio 129,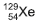 , obtido a partir do decaimento do iodo radiativo 129,
, obtido a partir do decaimento do iodo radiativo 129,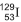 , que não existe mais nesse planeta.
(CLAUDE; STEPHEN, 2013, p. 13).
, que não existe mais nesse planeta.
(CLAUDE; STEPHEN, 2013, p. 13). Considerando-se as informações e os conhecimentos sobre estrutura atômica e radioatividade, é correto afirmar:

A nova Tabela Periódica, atualizada em março de 2017 pela
IUPAC, contém os nomes e símbolos dos elementos químicos
niônio113, moscóvio115, tennessínio117 e oganessônio118,
em homenagem aos pesquisadores e descobridores
japoneses, russos e americanos. Os novos elementos são
transactinoides de existência efêmera, de frações de segundos
e foram sintetizados nos aceleradores de partículas. Assim,
completam o sétimo período da Tabela. A equipe de
pesquisadores do niônio113, vai em busca do 119 e de suas
propriedades, o primeiro elemento químico do oitavo período.
As propriedades periódicas dos elementos químicos,
organizados em grupos e períodos, estão relacionadas aos
números atômicos e configurações eletrônicas. As tendências
dessas propriedades são verificadas em um grupo ou de um
grupo para o outro, ou entre elementos de um período.

A partir dessas informações, é correto afirmar:
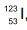 , e iodo-131,
, e iodo-131, 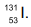 (http://www.cnen.gov.br/radiofarmacos. Adaptado)
(http://www.cnen.gov.br/radiofarmacos. Adaptado)
Os átomos de iodo-123 e iodo-131 possuem
( ) Sua distribuição eletrônica é [Kr] 4f14 5d10 6s26p4 . ( ) Trata-se de um elemento transurânico. ( ) Sua radiação pode ser detida por uma folha de papel. ( ) Só é letal quando ingerido ou inalado. ( ) É mais eletronegativo do que o selênio e o telúrio.
A sequência correta, de cima para baixo, é:
Com relação a esse metal ou a um de seus compostos, pode-se afirmar corretamente que


