Questões de Vestibular
Sobre relações da química com as tecnologias, a sociedade e o meio ambiente em química
Foram encontradas 364 questões

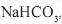 e ácido sulfúrico,
e ácido sulfúrico,  . No interior do extintor, essas duas substâncias fcam separadas, uma da outra. Para ser usado, o extintor deve ser virado de cabeça para baixo, a fm de possibilitar a mistura dos compostos, que, então, reagem entre si.
. No interior do extintor, essas duas substâncias fcam separadas, uma da outra. Para ser usado, o extintor deve ser virado de cabeça para baixo, a fm de possibilitar a mistura dos compostos, que, então, reagem entre si. Um dos produtos dessa reação é um gás, que produz uma espuma não-infamável, que auxilia no combate ao fogo.
Considerando-se essas informações, é CORRETO afrmar que a substância gasosa presente na espuma não-infamável é
Alguns dos processos físicos, químicos e bioquímicos que ocorrem com o mercúrio, após seu lançamento no ambiente, estão representados nesta figura:
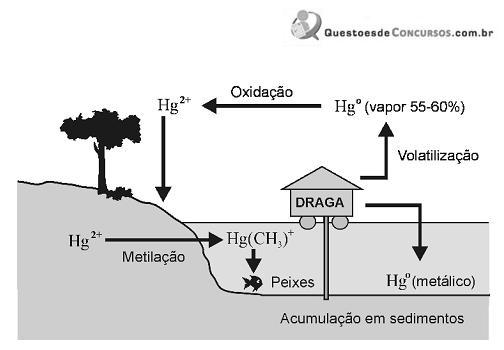
Considerando-se as informações fornecidas por essa figura e outros conhecimentos sobre o assunto, é CORRETO afirmar que