Questões de Vestibular de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Foram encontradas 53 questões
A relação entre essas energias é dada por:

Considerando as informações acima, julgue os itens 50 e 51, assinale a opção correta no item 52, que é do tipo C, e faça o que se pede no item 53, que é do tipo D.
Os fogos de artifício são dispositivos envolvidos em um cartucho de papel. Na parte inferior, está a carga explosiva, que dispara os fogos para o alto. O propelente mais utilizado é a pólvora negra, uma mistura de nitrato de potássio, enxofre e carvão. Para a produção de fogos coloridos, misturam-se sais de diferentes metais à pólvora. Elétrons dos metais, quando são excitados pelo calor, emitem, ao retornarem a níveis de energia mais baixos, radiação eletromagnética de diferentes cores. Na tabela abaixo, são listados alguns metais e a coloração característica que deles pode ser emitida.

A seguir, é apresentada uma reação da pólvora, sem balanceamento e sem os estados físicos das substâncias.

Tendo como referência as informações acima, julgue os itens seguintes.
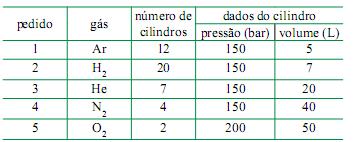
Sabendo que os cilindros rígidos e fechados estão armazenados na mesma condição de temperatura, o pedido que tem maior quantidade de matéria, em mol de gás, é o de número

Considerando-se que os cilindros I e II estão à temperatura de 27ºC e que os gases contidos no seu interior, respectivamente, CO2(g), N2(g) e He(g), se comportam como ideais, é correto afirmar:
Se, em repouso, uma pessoa consome 0,34 L de oxigênio por minuto, então o aumento da temperatura do ar resultará em massa menor de oxigênio consumido por minuto pela pessoa, o que explica o fato de ser mais difícil se respirar em dias muito quentes.
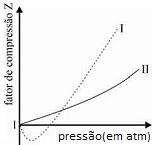
Considere que os gases da natureza, que são chamados de gases reais, tenham propriedades diferentes daquelas preditas pela lei dos gases ideais. Considere, ainda, o fator de compressão Z, que é a razão entre o volume molar do gás real e o volume molar de um gás ideal nas mesmas condições. Nesse caso, é correto afirmar que, no gráfico a seguir, da variação de Z em função da pressão, as curvas I e II representam, respectivamente, o comportamento dos gases NH3 e H2.
I. Apresenta massa molar igual a 90,2 g/mol.
II. Apresenta maior pressão de vapor do que a água, nas mesmas condições.
III. É menos densa que o ar, nas mesmas condições.
São corretas as afirmações contidas em
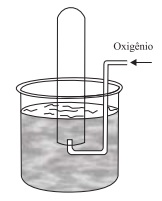
Quando o nível da água dentro do tubo de ensaio é o mesmo que o nível de fora, a pressão no interior do tubo é de 0,86 atm. Dadas a pressão de vapor (H2O) a 27 °C = 0,040 atm e R = 0,082 atm·L·K–1 ·mol –1 , o volume de gás, em mL, dentro do tubo de ensaio é igual a
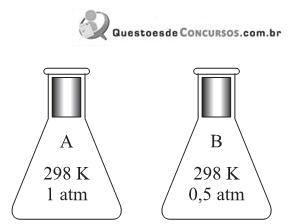
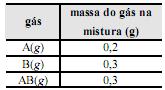
Sobre esses gases, são feitas as seguintes afirmações:
I. O frasco A apresenta o dobro de moléculas em relação ao frasco B.
II. O número de átomos do frasco B é o dobro do número de átomos do frasco A.
III. Ambos os frascos, A e B, apresentam a mesma massa.
IV. Considerando que a reação ocorreu por completo, o frasco C ainda contém gás oxigênio.
São corretas as afirmações

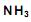 produzido a partir de 28 kg de
produzido a partir de 28 kg de 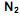 é:
é: 

