Questões de Vestibular
Sobre sistemas gasosos - lei, teoria cinética, equação e mistura dos gases. princípio de avogadro. em química
Foram encontradas 230 questões
DADOS QUE PODEM SER USADOS NESTA QUESTÃO

2H2(g) + O2(g)→ 2H2O(v)
CO(g) + O2 (g) ⟷ CO2(g)
A hemoglobina (Hb) é a proteína responsável pelo transporte de oxigênio. Nesse processo, a hemoglobina se transforma em oxihemoglobina (Hb(O2)n). Nos fetos, há um tipo de hemoglobina diferente da do adulto, chamada de hemoglobina fetal. O transporte de oxigênio pode ser representado pelo seguinte equilíbrio:
Hb + nO2 ⇌ Hb(O2)n ,
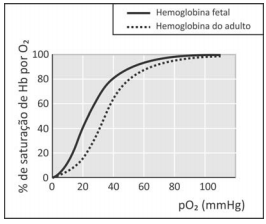
em que Hb representa tanto a hemoglobina do adulto quanto a hemoglobina fetal. A figura mostra a porcentagem de saturação de Hb por O2 em função da pressão parcial de oxigênio no sangue humano, em determinado pH e em determinada temperatura.
A porcentagem de saturação pode ser entendida como:
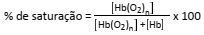
Com base nessas informações, um estudante fez as seguintes afirmações:
I. Para uma pressão parcial de O2 de 30 mmHg, a hemoglobina fetal transporta mais oxigênio do que a hemoglobina do adulto.
II. Considerando o equilíbrio de transporte de oxigênio, no caso de um adulto viajar do litoral para um local de grande altitude, a concentração de Hb em seu sangue deverá aumentar, após certo tempo, para que a concentração de Hb(O2)n seja mantida.
III. Nos adultos, a concentração de hemoglobina associada a oxigênio é menor no pulmão do que nos tecidos.
É correto apenas o que o estudante afirmou em
Note e adote:
pO2 (pulmão) > pO2 (tecidos).
Nas mesmas condições de pressão e temperatura, 50 L de gás propano (C3H8) e 250 L de ar foram colocados em um reator, ao qual foi fornecida energia apenas suficiente para iniciar a reação de combustão. Após algum tempo, não mais se observou a liberação de calor, o que indicou que a reação haviase encerrado. Com base nessas observações experimentais, três afirmações foram feitas:
I. Se tivesse ocorrido apenas combustão incompleta, restaria propano no reator.
II. Para que todo o propano reagisse, considerando a combustão completa, seriam necessários, no mínimo, 750 L de ar.
III. É provável que, nessa combustão, tenha se formado fuligem.
Está correto apenas o que se afirma e
Note e adote:
Composição aproximada do ar em volume: 80% de N2 e 20% de O2.
Com relação a princípios da química, julgue o próximo item.
Considere que 1 K = 1 ° C + 273, se o ar no interior de um pneu está a 15 ° C sob a pressão de 5 atm, então a pressão será maior que 5,5 atm quando o ar estiver a 38 ° C.
A respeito das substâncias e de suas transformações químicas, julgue o item a seguir.
Mantendo o volume constante, a pressão de um gás ideal aumentará se houver aumento da temperatura.
O gás hidrogênio foi usado no dirigível rígido Graff Zeppelin. Já o gás hélio é atualmente usado nos dirigíveis semirrígidos e não rígidos.
Sobre esses gases, é CORRETO afirmar que ambos são
(Dados: N = 14 g.mol-1; H = 1 g.mol-1; R = 0,082 atm.L.mol-1.K-1)
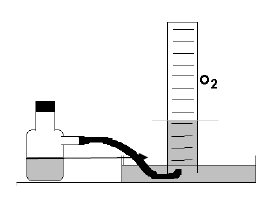
Água oxigenada contém peróxido de hidrogênio (H2O2), que, com o uso de um catalisador, se decompõe, produzindo gás oxigênio e água, conforme a equação abaixo.
H2O2 H2O + ½ O2
Um grupo de estudantes fizeram essa experiência, usando 100 mL de água oxigenada, coletando o gás oxigênio obtido sobre água, conforme ilustrado pela figura, obtendo 1,17 L de gás oxigênio, medidos a uma pressão atmosférica de 0,91atmosferas e a uma temperatura de 20 oC .
Usando a equação PV=nRT, conseguiram determinar o número de mols de O2 obtido e, consequentemente, o número de mols de H2O2 contidos no volume de água oxigenada utilizada. Dessa forma, puderam também determinar a massa deH2O2 contidos nessa água oxigenada. Diante do exposto, pode se concluir que a percentagem m/v (massa volume) deH2O2 na água oxigenada é:
Dados: Constante dos gases ideais R=0,082 atm.L/mol.KK = 273 + t (oC)
Fe(s) + 2 HCl(aq) → FeCl2(aq) + H2(g)
Então, na temperatura de 25 ºC e pressão de 1 atm, o volume de gás hidrogênio, considerado gás ideal, para inflar o balão foi de aproximadamente:
Dados:
Massas Molares (g.mol-1): H = 1,0; Cl = 35,5 e Fe = 56,0; R = 0,082 L.atm.K-1.mol-1 (Constante Universal dos Gases); T (K) = T(ºC) + 273.
Assim, considerando-se que um recipiente de vidro aberto, inicialmente, contendo ar a 27°C, é aquecido a 127°C e mantido a essa temperatura, no ambiente em que está, pode-se corretamente afirmar:
Assim, considerando-se 100,0g de uma amostra de gases ideais, que contém 64% de SO2, e 36% de He, em massa a 27°C, a 1,0atm, no interior de um recipiente, é correto afirmar:
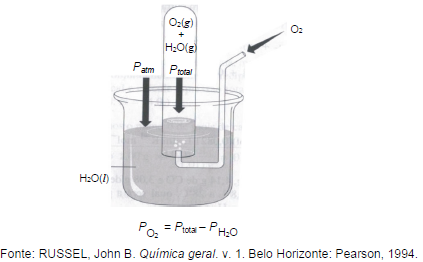
Supondo que nesse experimento 6,4 g de gás oxigênio (O2) é coletado sobre a água a 35ºC e a pressão total é de 0,980atm, o volume aproximado, em litros, que o gás irá ocupar é? Dados (pH2O = 0,056; R = 0,082)
Admitindo-se que a massa molar média do ar é 28,9 g/mol e com base nessas equações, é correto afirmar que
“A principal hipótese para o balão ter explodido e pegado fogo é que ele foi enchido com um gás impróprio para essa finalidade. O mais recomendado é o hélio, porque não pega fogo ou explode. Porém, pelo alto preço, algumas pessoas usam outros gases como butano [C4 H10] e hidrogênio [H2 ], o que pode causar vários acidentes”.
(Disponível em: http://g1.globo.com/goias/noticia/2016/05/mae-nao-pensava-quebalao-pudesse-explodir-e-queimar-filho-bomba.html. Acessado em 21/08/2016)
A notícia aponta dois gases como possíveis substitutos do gás hélio no balão flutuante que explodiu. O problema das possibilidades apontadas é que:


