Questões de Vestibular
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 991 questões
Um estudante foi ao laboratório e realizou uma série de experimentos para identificar um determinado composto químico. As observações sobre esse composto estão descritas abaixo:
Observação 1 - Possuía propriedades corrosivas.
Observação 2 - Possuía alta solubilidade em água.
Observação 3 - O papel de tornassol ficou vermelho em contato com ele.
Observação 4 - Apresentou condução de correte elétrica quando dissolvido em água.
Baseado nas observações feitas pelo estudante, pode-se afirmar que o composto analisado é:
A história de contaminações por metais (rejeitos) das águas dos rios em Minas Gerais é antiga. Segundo informações de pesquisa da Unicamp, há 15 anos, o arsênio no solo e na água utilizada por moradores do Quadrilátero Ferrífero estaria relacionado à intensa mineração de ouro, explorada nos últimos 300 anos.
O arsênio está entre os metais mais nocivos à saúde humana. Quantidades elevadas (acima de 10-5 gramas por litro de água potável) podem provocar vários tipos de cânceres, além de abalos ao sistema nervoso, malformação neurológica e abortos.
(Fonte: Isabel Gardenal, Jornal da Unicamp, novembro de 2002.)
Sobre o arsênio e as informações apresentadas são feitas algumas afirmações. Assinale a correta:
COOH
Ácido Cítrico
O ácido cítrico, responsável pela acidez das frutas cítricas, é utilizado como acidificante e flavorizante no processamento de alguns alimentos.
A partir dessas informações, é correto afirmar:
Ácido Halogenídrico Constante de ionização, Ka, a 25º C
HF (aq) 6,0.10-4
HC (aq) 1,0.107
HBr (aq) 1,0.109
HI (aq) 3,0.109
A tabela relaciona os valores da constante de ionização, Ka, dos ácidos halogenídricos.
A partir da análise dessa tabela, é correto afirmar:
I. CaC2(s) + N2(g) 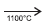 CaNCN(s) + C(s)
CaNCN(s) + C(s)
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando carbeto de cálcio, CaC2, é aquecido em um forno elétrico, na presença de nitrogênio atmosférico, a 1100ºC, dá origem à cianamida de cálcio, empregada largamente como fertilizante nitrogenado de ação lenta, pois leva alguns meses, no solo, para se hidrolisar de acordo com a equação química II. Como a cianamida de cálcio não é arrastada pelas chuvas, é um fertilizante melhor do que o nitrato de amônio, NH4NO3, e a ureia, CO(NH2)2.
Uma análise dessas informações permite afirmar:
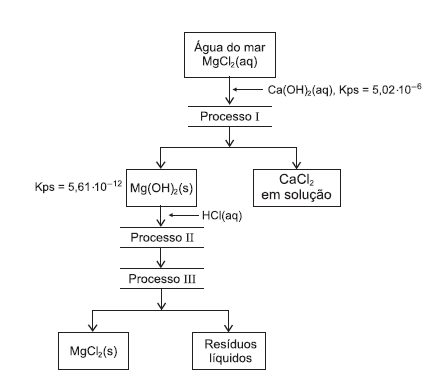
No processo Dow, de extração de magnésio, da água do mar, sob a forma de íons Mg2+(aq), representado pelo fluxograma, hidróxido de cálcio, Ca(OH)2(aq), é adicionado à água do mar, para que o Mg(OH)2(s) se precipite, permanecendo os íons Ca2+(aq) na fase aquosa. Após precipitação do cloreto de magnésio, MgCl2(s), produto final desse processo, esse sal é utilizado para produzir magnésio por eletrólise.
A partir da análise desse fluxograma e das informações do
texto, é correto afirmar:
A partir dessa informação, é correto afirmar:
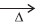 Na4P2O7(s) + 2CO2(g) + 2H2O(ℓ)
Na4P2O7(s) + 2CO2(g) + 2H2O(ℓ) A mistura de dihidrogeno-pirofosfato de sódio com hidrogenocarbonato de sódio, de acordo com a equação química, é utilizada como fermento químico na produção industrial de bolos, pães e biscoitos. Essa é uma forma rápida de fazer expandir, durante o aquecimento, a massa para o preparo desses alimentos, em relação à utilizada com fermento biológico.
Considerando-se essas informações, é correto afirmar:
O dihidrogenofosfato de sódio, NaH2PO4, é um conservante utilizado em alimentos.
Em relação a esse conservante, é correto afirmar:
A cachaça Havana é a mais famosa do Brasil e uma das precursoras da valorização da cachaça artesanal em todo o mundo. Produzida em Salinas-MG, desde 1943, é envelhecida por cerca de oito anos em tonéis de bálsamo. Relatos contam que os funcionários do alambique recebiam garrafas de cachaça Havana como pagamento dos seus salários. Depois, trocavam no mercado pelos produtos de que necessitavam. Com produção limitada, tornou-se rara no mercado, sendo disputada por degustadores e colecionadores do país e do exterior.
Sabendo que o rótulo da garrafa de 600 mililitros da cachaça Havana informa que seu teor alcoólico é de 47%, assinale a alternativa CORRETA.
Determinada água mineral apresenta o seguinte rótulo:

(Disponivel em: https://cdlcenter.com/agua-mineral-viva-20lt-comgarrafao/produto/19198-0-0. Acesso em 28 de agosto de 2016)
Analisando o rótulo da água apresentado, é INCORRETO
afirmar:

 I. Ao beber 960 mL de suco de acerola natural, o atleta
ingeriu menos calorias que se tivesse tomado 240 mL de
suco de maçã natural.
II. Ao beber 960 mL de suco de acerola natural, o atleta
ingeriu mais calorias que se tivesse tomado 240 mL de suco
de maçã natural.
III. Ao tomar 500 ml de água de coco, o atleta ingeriu
aproximadamente 129 calorias.
IV. Ao beber 4 copos de suco de tomate natural, o atleta ingeriu
menos calorias que se tivesse tomado 1 copo de suco
manga natural.
Estão corretas:
I. Ao beber 960 mL de suco de acerola natural, o atleta
ingeriu menos calorias que se tivesse tomado 240 mL de
suco de maçã natural.
II. Ao beber 960 mL de suco de acerola natural, o atleta
ingeriu mais calorias que se tivesse tomado 240 mL de suco
de maçã natural.
III. Ao tomar 500 ml de água de coco, o atleta ingeriu
aproximadamente 129 calorias.
IV. Ao beber 4 copos de suco de tomate natural, o atleta ingeriu
menos calorias que se tivesse tomado 1 copo de suco
manga natural.
Estão corretas: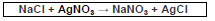
Analise a reação, e assinale a alternativa correta

Nessa situação, é CORRETO afirmar que:
I - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a temperatura de ebulição da solução seja superior à do solvente.
II - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a temperatura de fusão da solução seja inferior à do solvente.
III - A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a pressão máxima de vapor da solução seja inferior à do solvente quando ambas são submetidas à mesma temperatura.
IV- A adição de um soluto, como o cloreto de sódio, em um solvente, como a água, de forma a criar uma solução, normalmente faz com que a pressão osmótica da solução seja superior à do solvente.

Apressão de vapor é uma importante propriedade físico-química das substâncias e das soluções.
Com base nos dados fornecidos e nos conhecimentos de química, é correto afirmar: