Questões de Vestibular
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 991 questões
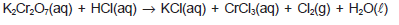
O dicromato de potássio reage com ácido clorídrico, de acordo com a equação química não balanceada apresentada.
Em relação a essa equação química e aos conhecimentos sobre classificação periódica, funções inorgânicas e reações químicas, pode-se afirmar:
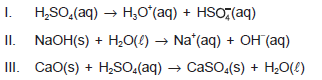
Com base nessas informações e nos conhecimentos sobre funções inorgânicas, reações químicas e soluções, pode-se afirmar:
PESQUISA GERA CACHAÇA “TIPO EXPORTAÇÃO”
Método ajuda a diminuir teor de cobre na bebida, vencendo regras do mercado internacional para consumo de destilados. Brasil permite até 5 mg/L do metal na aguardente, mas a Europa exige um máximo de 2 mg/L; a técnica não muda o sabor ou o aroma do produto.
[...] Para retirar o metal da bebida, os pesquisadores [...] misturaram à cachaça recém-destilada mármore ou calcário em pó, ambos formados basicamente por carbonato de cálcio. [...] é como se o carbonato “largasse” o cálcio e agarrasse o cobre, formando um precipitado - uma espécie de pó, que é facilmente retirado por uma filtragem. “Conseguimos fazer que uma bebida que tinha 20 mg/L de cobre chegue a 2 mg/L”, diz Oliveira.
Disponível em: http://www.ufcg.edu.br/prt_ufcg/assessoria_impre nsa/mostra_noticia.php?codigo=2905. Acesso em: 16 de agosto de 2015.
[Dados: M(Ca) = 40 g/mol; M(Cu) = 63,5 g/mol.]
A análise dos dados permite inferir que
A imagem a seguir é a fotografia de uma impressão digital coletada na superfície de um pedaço de madeira. Para obtê-la, foi utilizada uma técnica baseada na reação entre o sal do suor NaCℓ, presente na impressão digital, com solução aquosa diluída de um reagente específico. Depois de secar em uma câmara escura, a madeira é exposta à luz solar.

Disponível em: guiadoestudante.abril.com.br. Acesso em: 15 de agosto 2015.
Sobre o processo químico descrito, é pertinente inferir
que a solução usada foi de
[...] “Solos ácidos, caracterizados por baixos valores de pH [...], teores insuficientes de cálcio e excesso de alumínio e/ou manganês, [...] limitam fortemente a produtividade das culturas, pois impedem absorção plena dos nutrientes pela plantas.” [...]
Disponível em: http://www.estadao.com.br/noticias/geral, e-hora-de-aplicar-calcario-no-solo,218382. Acesso em: 15 de agosto de 2015.
Para tornar o solo adequado a uma boa produtividade, pode-se inferir que o agricultor deverá usar
CLORETO DE MAGNÉSIO
O cloreto de magnésio pode ser utilizado para complementar os baixos níveis de magnésio no sangue em pessoas que tomam medicamentos ou sofrem de doenças que inibem a sua capacidade de absorver magnésio na dieta. [...] Os sintomas de deficiência de magnésio incluem anorexia, náuseas, vômitos, fadiga, fraqueza, dormência, formigamento, contrações musculares, câimbras, convulsões, alterações de personalidade, arritmia e espasmos coronários. O magnésio é essencial em mais de 300 reações bioquímicas no corpo e desempenha um papel importante nos músculos, nos nervos e na função imunológica, impedindo a arritmia, dando força aos ossos, na regulação do açúcar no sangue e em níveis de pressão arterial, no metabolismo energético e na síntese de proteínas.
Disponível em: http://www.saudemelhor.com/cloreto-magnesio-praque-serve-efeitos-colaterais/. Acesso em: 11 de agosto de 2015.
Sobre a substância destacada no texto, é pertinente inferir que
Observe a escala abaixo:

O suco extraído do repolho roxo pode ser utilizado como indicador do caráter ácido (pH entre 0 e 7) ou básico (pH entre 7 e 14) de diferentes soluções. Misturando-se um pouco de suco de repolho e da solução, a mistura passa a apresentar diferentes cores, segundo sua natureza ácida ou básica, de acordo com a escala acima, que relaciona a cor final do sistema substância + indicador com o pH aproximado que ela possui. Ao testar algumas soluções com o suco de repolho roxo, foram obtidos os seguintes resultados:
- Amoníaco: verde
- Leite de magnésia: azul
- Vinagre: vermelho
- Leite de vaca: rosa
Com base nessas informações, as substâncias amoníaco, leite de magnésia, vinagre e
leite de vaca têm caráter respectivamente:
Uma das substâncias abaixo que possui caráter ácido é
20°C 30°C 40°C 50°C Solubilidade do KNO3 por 100 g de água 31,6g 45,8g 63,9 85,5
De acordo com os dados acima, para diminuir o precipitado de fundo devemos:
Um estudante de Engenharia Química pipeta 50mL de solução aquosa 0,02mol/L de ácido clorídrico e transfere para um balão volumétrico de 1000mL, ajustando-se para esse volume a solução final, usando água pura.
O pH da solução final é igual a

A preocupação com o diabetes e a obesidade fez surgir os adoçantes artificiais, em substituição ao açúcar. Entretanto a utilização crescente desses produtos criou outros problemas, a exemplo da possibilidade de causar câncer e até mesmo obesidade, além de contribuir com o aumento de ingestão de íons sódio, Na+ , segundo alguns especialistas, que não deve ultrapassar a 1200mg. Um desses produtos, ciclamato de sódio, um adoçante artificial 30 vezes mais doce que a sacarose, apresenta, no rótulo, as informações adaptadas, em destaque, na tabela.
A partir das informações do texto e dos dados da tabela, é correto afirmar:
Massas molares, em g/mol: H = 1, O = 16, Cl = 35,5