Questões de Vestibular
Sobre transformações químicas: elementos químicos, tabela periódica e reações químicas em química
Foram encontradas 730 questões

Alimentos como ovos, leite, manteiga e cacau fornecem ao organismo uma substância chamada ergosterol. Na presença de raios solares, nosso organismo transforma ergosterol em vitamina D. Essa vitamina favorece a retenção de Cálcio e de Fósforo nos ossos e nos dentes (REIS, Martha. Completamente Química: Vol. 1. São Paulo: FTD, 2001. p. 390). Dado que a massa molar do ergosterol e da vitamina D (calciferol) são 396,6 g mol–1 e 384,6 g mol–1, respectivamente, assinale o que for correto.

Alimentos como ovos, leite, manteiga e cacau fornecem ao organismo uma substância chamada ergosterol. Na presença de raios solares, nosso organismo transforma ergosterol em vitamina D. Essa vitamina favorece a retenção de Cálcio e de Fósforo nos ossos e nos dentes (REIS, Martha. Completamente Química: Vol. 1. São Paulo: FTD, 2001. p. 390). Dado que a massa molar do ergosterol e da vitamina D (calciferol) são 396,6 g mol–1 e 384,6 g mol–1, respectivamente, assinale o que for correto.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Sabendo-se que o astrônomo amador preencheu seu balão com uma quantidade de x gramas de gás hidrogênio, se o mesmo utilizasse 2x gramas desse gás no mesmo balão, este alcançaria uma altura muito maior antes de estourar.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Os dirigíveis muito utilizados antigamente em transporte aéreo eram considerados bombas aéreas, pois continham gás hélio, que é extremamente inflamável.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
O astrônomo amador poderia utilizar gases, como o hidrogênio, o hélio ou o nitrogênio, para encher e fazer voar o seu balão.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
De modo geral, o volume atômico cresce e decresce da mesma maneira que o raio atômico, na tabela periódica.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Um elemento que apresenta seus elétrons mais externos, em um nível P, possui maior ponto de fusão do que um elemento que apresenta seus elétrons mais externos, em um nível L.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Num mesmo período, um metal alcalino terroso possui menor raio atômico do que um metal alcalino.
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

*OS VALORES DAS MASSAS ATÔMICAS DOS ELEMENTOS FORAM ARREDONDADOS PARA FACILITAR OS CÁLCULOS. ESTA TABELA PERIÓDICA É EXCLUSIVA PARA ESTE VESTIBULAR E NÃO DEVE SER UTILIZADA PARA OUTRAS FINALIDADES.
Os calcogênios possuem maior densidade (ou densidade absoluta) do que os halogênios.
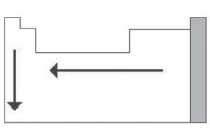
Indique qual propriedade periódica é representada pela figura abaixo.
I. O elemento químico de número atômico 30 tem 3 elétrons de valência. II. Na configuração eletrônica do elemento químico com número atômico 26 há 6 elétrons no subnível 3d. III. 3s23p3 corresponde a configuração eletrônica dos elétrons de valência do elemento químico de número atômico 35. IV. Na configuração eletrônica do elemento químico de número atômico 21 há 4 níveis energéticos.
Estão corretas, SOMENTE:
1s2 2s2 2p6 3s2 3p10 4s6 3d10 4p6 5s2 4d1 , o número de camadas e o número de elétrons mais energéticos para o ítrio, serão respectivamente:
A partir dessas informações e com base nas propriedades periódicas e de alguns compostos de manganês, é correto afirmar: