Questões de Vestibular MACKENZIE 2010 para Vestibular
Foram encontradas 60 questões
Dada a matriz  , o determinante da matriz inversa
de A é
, o determinante da matriz inversa
de A é
Terremoto arrasa país mais pobre das Américas

O terremoto atingiu o Haiti no dia 12 de janeiro de 2010. O país é um dos mais pobres do mundo, com 80% da população vivendo abaixo da linha de pobreza, com menos de US$ 2,00 (R$ 3,50) por dia, por habitante. Também possui índices recordes de mortalidade infantil, desnutrição e contaminação por AIDS.
Com relação ao Haiti e ao terremoto que o afligiu, assinale a alternativa correta.
I. Uma das justificativas para a sua construção foi a de que a interiorização da capital traria desenvolvimento para áreas despovoadas e inexploradas do território brasileiro, além de ser menos vulnerável a ataques externos.
II. Após a sua construção, municípios periféricos (cidades satélites) foram criados pelo governo, visando atender às necessidades sóciourbanas da população trabalhadora que, via de regra, se empregava em Brasília.
III. A capital passou a ser polo de atração para migrantes. Atualmente, a região Centro-Oeste abriga mais de 13 milhões de habitantes.
Estão corretas
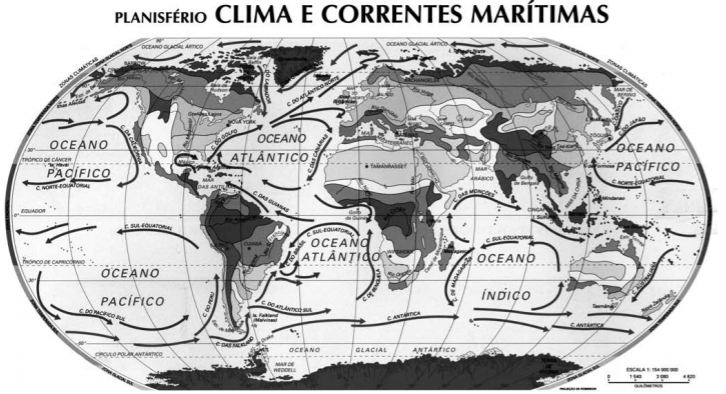
Fonte: Geoatlas, Maria Elena Simielli
Observando o mapa, considere as afirmações I, II e III abaixo.
I. A corrente de Humboldt, no Hemisfério Sul, é muito fria, ocasionando queda da temperatura nas áreas litorâneas, o que favorece o fenômeno da ressurgência e a formação do deserto de Atacama.
II. A corrente da Califórnia é quente, o que colabora com as altas temperaturas nas porções litorâneas, onde aparecem as estepes. É, ainda, responsável também pela formação do deserto da Califórnia.
III. A corrente do Golfo, por ser quente, impede o congelamento do Mar do Norte e ameniza os rigores climáticos do inverno na porção ocidental da Europa.
Dessa forma,

Savana Brasileira
De acordo com os seus conhecimentos e as definições do Profº Aziz Ab’Saber, assinale a alternativa correta relativa ao domínio morfoclimático ilustrado.
I. uma continuidade do processo de queda da taxa de fecundidade e um aumento do percentual da população jovem em decorrência disso.
II. a confirmação de que a violência urbana é um fenômeno preocupante e que explica, por si só, a contínua redução da expectativa de vida verificada nas últimas quatro décadas.
III. a manutenção do processo de redução dos índices de natalidade, que tem ocorrido desde o fim da década de 1970, e que resulta, entre outros fatores, no aumento do acesso a métodos contraceptivos, mesmo entre as camadas mais pobres da população.
IV. a elevação da proporção de idosos em decorrência da ampliação do acesso a serviços de saúde e saneamento, que tem determinado o aumento da longevidade.
Estão corretas, apenas,
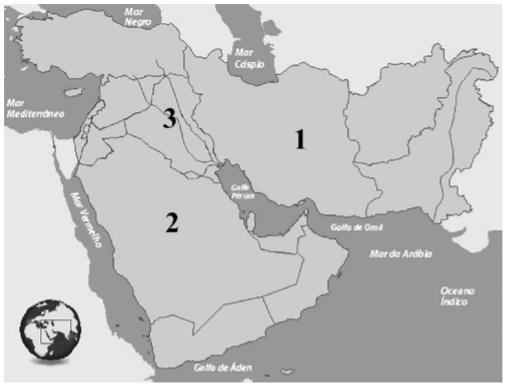
Observando o mapa, assinale a alternativa correta.

Mapa de trens e metrô de São Paulo, Brasil
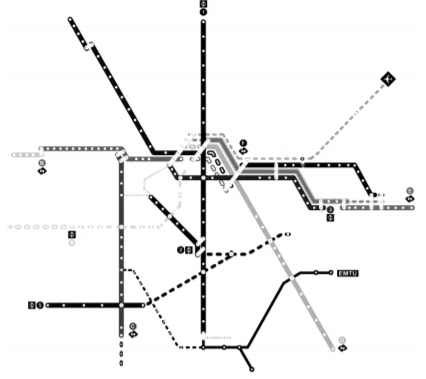
I. Os dois mapas mostram a presença de transportes coletivos de massa. Desse modo, a mobilidade urbana e a densidade das linhas ilustradas se assemelham, revelando as prioridades das duas cidades para os transportes coletivos.
II. O traçado das linhas observadas em Moscou e a densidade desse tipo de transporte são mais intensos do que em São Paulo, fato que demonstra prioridades diferenciadas das duas cidades em relação aos transportes coletivos.
III. Moscou tem um traçado que permite tanto a circulação pelas áreas centrais quanto a comunicação no entorno delas, o que facilita a mobilidade urbana, fato não observado com a mesma intensidade em São Paulo.
IV. O Metrô de São Paulo é mais moderno e mais limpo do que o de Moscou, fato que nos permite afirmar que a cidade brasileira tem maior eficiência no setor, pois os traçados das linhas e a sua extensão pouco interferem na mobilidade urbana de uma grande cidade.
Estão corretas, apenas,
A adição de sulfato de alumínio é o primeiro passo desse processo e pode ser representado pela equação química NÃO BALANCEADA abaixo.
Aℓ2(SO4)3 + H2O
 Aℓ(OH)3 + H2SO4
Aℓ(OH)3 + H2SO4
Assim, de acordo com a equação dada, de adição de sulfato de alumínio, é correto afirmar que
Dado: massa molar em (g/mol) H = 1, O = 16, Aℓ = 27 e S = 32.
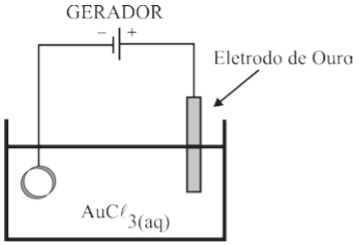
Dados: Au = 197 g/mol e 1 mol de elétrons = 9,6∙104 C.
A respeito do processo eletroquímico ilustrado acima, considere as afirmações dadas, de I a V.
I. O anel foi colocado no ânodo da cuba eletrolítica.
II. Ao passar uma corrente de 3 ampères, durante 16 minutos, há a deposição de aproximadamente 2,0 g de ouro sobre o anel.
III. No polo positivo ocorre a reação Au(s) → Au3+(aq) + 3 e-.
IV. No cátodo da cela eletrolítica ocorre oxidação.
V. No anel ocorre a reação Au3+(aq) + 3 e- → Au(s).
Dessas afirmações, estão corretas, somente
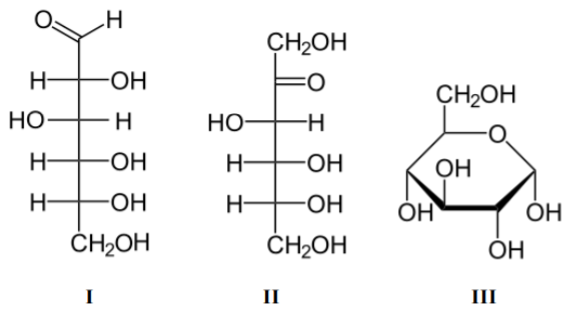
A glicose é um monossacarídeo de grande importância biológica, pois as células a usam como fonte de energia. É um cristal sólido de sabor adocicado, de fórmula molecular C6H12O6, encontrado na natureza na forma livre ou combinada. Juntamente com a frutose, é o carboidrato fundamental na formação do dissacarídeo sacarose. A molécula de glicose pode existir em forma de cadeia aberta ou cíclica, sendo que tais formas permanecem em equilíbrio. Representadas as estrututuras da D-glicose em cadeia aberta (I), D-frutose (II) e D-glicose cíclica (III), respectivamente, é INCORRETO afirmar que
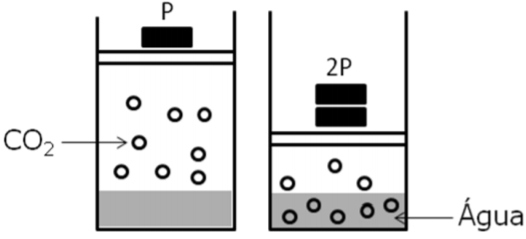
No champanhe, nos vinhos espumantes e nas cervejas, o dióxido de carbono (CO2) é o principal responsável pela formação das bolhas, originadas quando o levedo fermenta os açúcares, convertendo-os em moléculas de álcool e de CO2.
Após o engarrafamento, é estabelecido um equilíbrio entre o gás carbônico dissolvido no líquido e o gás que está no espaço sob a rolha ou a tampa.
Considerando as informações do texto, os seus conhecimentos químicos e a figura dada, é INCORRETO afirmar que
I. C(graf) + O2(g) → CO2(g) ΔH°= – 394 kJ/mol
II. H2(g) + 1/2 O2(g) → H2O(ℓ) ΔH° = – 242 kJ/mol
III. C(graf) + 2 H2(g) → CH4(g) ΔH° = – 74 kJ/mol
IV. 2 C(graf) + 3 H2(g) + 1/2 O2(g) → C2H5OH(ℓ) ΔH° = – 278 kJ/mol
É correto afirmar que
N2(g) + 3 H2(g)
Com o intuito de favorecer a produção de amônia, foram feitas, no sistema, as intervenções de I a V.
I. Aumento da pressão total do sistema.
II. Aumento da pressão parcial do gás amônia.
III. Diminuição da concentração do gás hidrogênio.
IV. Aumento da concentração do gás nitrogênio.
V. Utilização de um catalisador de ferro metálico.
São eficientes, para esse propósito, apenas as intervenções
As reações que acontecem no interior da bateria estão representadas abaixo.
Ânodo: Pb(s) + HSO4-(aq) + H2O(ℓ) → PbSO4(s) + H3O+(aq) + 2e- Cátodo: PbO2(s) + 3H3O+(aq) + HSO4-(aq) + 2e- → PbSO4(s) + 5H2O(ℓ)
A respeito das baterias de chumbo, considere as afirmações I, II, III e IV.
I. A concentração da solução de ácido sulfúrico utilizada na bateria é de aproximadamente 390 g/L. II. Um derramamento da solução de bateria pode ser neutralizado com uma solução de cloreto de amônio. III. Uma solução de bateria pode ser preparada a partir da diluição de 100 mL de ácido sulfúrico, 18 mol/L, com água pura, até volume final de 1 L. IV. A equação Pb(s) + PbO2(s) + 2H3O+(aq) + 2 HSO4-(aq) → 2 PbSO4(s) + 4H2O(ℓ) representa a reação global que ocorre na bateria.
Dado: massa molar do H2SO4 = 98 g/mol.
Dessas afirmações, estão corretas, apenas