Foi proposto a um grupo de alunos um experimento sobre a re...
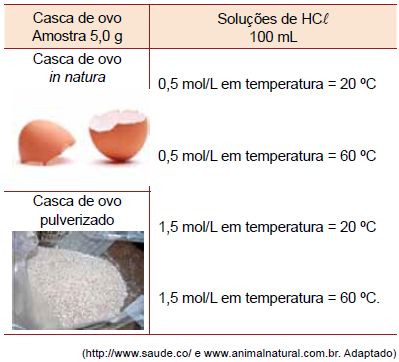
O experimento consistia em medir o tempo da reação da solução ácida com a amostra de casca de ovo. Para a preparação do experimento, foi removida a película de material orgânico que compõe a casca de ovo, tanto para o seu uso in natura como para preparação da amostra em pó.
A combinação que apresentou o menor tempo de reação foi aquela que usou
- Gabarito Comentado (1)
- Aulas (5)
- Comentários (2)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
• Concentração dos reagentes: o aumento da concentração dos reagentes é capaz de elevar o número de colisões efetivas e, consequentemente, a velocidade da reação;
• Temperatura: o aumento da temperatura promove um aumento da energia cinética (agitação das moléculas), o que também resulta em um aumento do número de colisões efetivas e, consequentemente, da velocidade da reação;
• Superfície de contato: o aumento da superfície de contato facilita e aumenta o número de colisões efetivas e, como resultado, a velocidade da reação também aumenta.
Com base no exposto e analisando o experimento realizado pode-se inferir que a reação com maior velocidade foi a que a apresentou as seguintes condições:
Maior concentração de HCl: 1,5 mol/L;
Maior temperatura: 60 °C;
Maior superfície de contato: casca de ovo em pó.
Gabarito do Professor: Letra A.
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
quanto maior a temperatura (60>20) e quanto maior a concentraçao do reagente (1,5 mol hcl>0.5 mol hcl), menor será o tempo da reaçao, ou seja, mais rapida ela será
FATORES DIRETAMENTE PROPORCIONAIS:
- TEMP.
- CONCENTRAÇÃO
- PRESSÃO
- SUPERFÍCIE
COMO É EM PÓ, TERÁ MAIOR SUPERFÍCIE DE CONTATO, POSSUI MAIOR TEMP (60) E MAIOR CONCENTRAÇÃO 1,5.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo