Questões de Vestibular
Foram encontradas 706 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
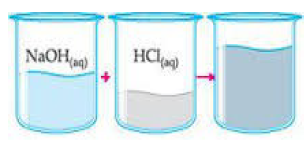
Ao se misturar 100 mL de HCl 1/mol/L com100 mL de NaOH de mesma concentração,obtém-se uma solução de NaCl (sal de cozinha) e observa-se claramente um aumento de temperatura.
Diante do exposto, pode-se afirmar que se trata de uma reação
N2(g) + 3 H2(g) ⇌ 2 NH3(g); ∆H < 0
Contudo, considerando em um determinado instante que o sistema esteja em equilíbrio, a produção de amoníaco será aumentada se:
Concentração de ácido acético: 6,0% m/V
Ao explicar que o vinagre é uma solução aquosa de ácido acético (ácido etanóico), o professor deixou o seguinte questionamento valendo um ponto na média: “Qual o pH do vinagre?” As seguintes informações foram fornecidas pelo professor:
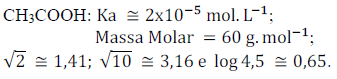
Assim, ganhará o ponto o aluno que responder que o pH é aproximadamente:
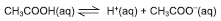
Dos sistemas em equilíbrio químico iônico em solução aquosa, um dos mais importantes é o que ocorre na ionização de ácidos e de bases, como o representado pela equação química, em que o ácido acético, em solução aquosa 0,1 mol.L–1, está 1,0% ionizado, à determinada temperatura.
Considerando-se essas informações, é correto afirmar:
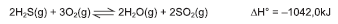
O deslocamento do equilíbrio químico de um sistema é toda e qualquer alteração de velocidade de reação direta ou inversa, que provoca modificações nas concentrações de substâncias químicas e, consequentemente, leva a um novo estado de equilíbrio.
A aplicação desse conceito de deslocamento de equilíbrio químico ao sistema representado pela equação química permite corretamente afirmar:
