Questões de Vestibular
Foram encontradas 69.760 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
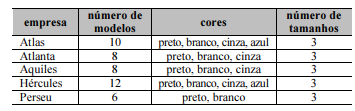
A chance de se adquirir um dos produtos da empresa Aquiles é inferior a 18%.

A chance de se adquirir qualquer um dos produtos, em qualquer modelo, cor ou tamanho, é inferior a 0,3%.

A chance de se adquirir o produto na cor preta é superior 0,38.
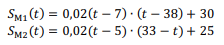
Assinale a opção correta no item que é do tipo C.
Assinale a opção que corresponde a um intervalo I tal que, para algum t ∈ I, SM1(t) = SM2(t).
B I = (30, 35)
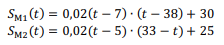
Para t = 17h, o modelo SM1 registrou um número de vendas superior ao modelo SM2.
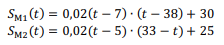
Tendo como base essas informações, julgue o item.
Para t > 62h, SM1(t) ≥ SM2(t).
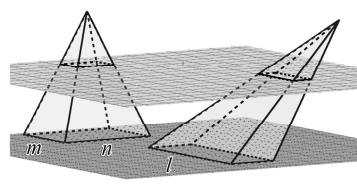
Faça o que se pede no item que é do tipo B.
Considerando l = 6 cm e h = 4 cm, calcule, em cm2 , o valor da área da superfície total da pirâmide regular. Após realizar todos os cálculos solicitados, despreze, para a marcação no Caderno de Respostas, a parte fracionária do resultado final obtido, caso ela exista.
096

Tendo o texto precedente como referência inicial, julgue o item.
Para m 1/2 e n = 2l, as duas pirâmides têm o mesmo volume.

Se h = 1/2, o apótema da pirâmide regular será igual a
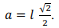

Tendo o texto precedente como referência inicial, julgue o item.
Um plano que intercepta a pirâmide regular na altura h/2 define um tronco de pirâmide cujo volume é 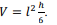 .
.
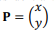 no plano, realizada pela
operação:
no plano, realizada pela
operação: 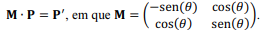
Para todo
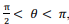 o vetor
o vetor 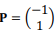 será rotacionado
para o quarto quadrante.
será rotacionado
para o quarto quadrante. 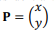 no plano, realizada pela
operação:
no plano, realizada pela
operação: 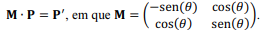
O determinante da matriz M é igual a 1.
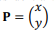 no plano, realizada pela
operação:
no plano, realizada pela
operação: 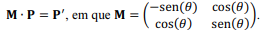
Para θ = π/2, a matriz R transforma o vetor
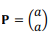 em
em 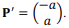
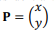 no plano, realizada pela
operação:
no plano, realizada pela
operação: 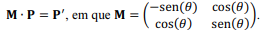
A matriz M permite que seja calculada a sua matriz inversa, dada por M -1 = - M.
A partir dessas informações, julgue o item a seguir.
Se m ≠ 0, então f ( - b/m) = 1.
A partir dessas informações, julgue o item a seguir.
Quando m < 0, o modelo representa uma função crescente.
A partir dessas informações, julgue o item a seguir.
A sequência f(x0), f(x0 + 1), f(x0 + 2), ..., f(x0 + n), em que n ∈ ℕ, é uma progressão geométrica de razão r = em.
A partir dessas informações, julgue o item a seguir.
Para m = −2 e b = 0, o gráfico da função h (x) = In [f (x)] será igual ao gráfico da reta y = 2x.
Para a testagem do módulo matemático de um sistema de IA, solicitou-se que ele gerasse, em um plano cartesiano xOy, uma circunferência que passa pelos pontos A = (5, 0), B = (0, 3) e C = (0, 10), e, em seguida, que descrevesse estratégias para que fosse encontrado o centro da circunferência por meio da utilização de régua e compasso. Como resposta, o sistema de IA forneceu a figura e as estratégias a seguir.
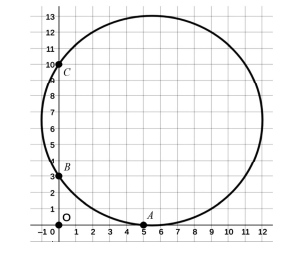
Estratégias:
• trace uma reta r que passe pelos pontos B e C;
• trace, no ponto C, uma reta s que seja perpendicular à reta r;
• denomine D o novo ponto em que a reta ; cruza a circunferência;
• ache o ponto médio do segmento 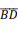 , que é o centro da circunferência, e o denomine E.
, que é o centro da circunferência, e o denomine E.
Calcule a área do triângulo ABC Multiplique o resultado por 10. Após efetuar todos os cálculos solicitados, despreze, para a marcação no Caderno de Respostas, a parte fracionária do resultado final obtido, caso ela exista.
175
Para a testagem do módulo matemático de um sistema de IA, solicitou-se que ele gerasse, em um plano cartesiano xOy, uma circunferência que passa pelos pontos A = (5, 0), B = (0, 3) e C = (0, 10), e, em seguida, que descrevesse estratégias para que fosse encontrado o centro da circunferência por meio da utilização de régua e compasso. Como resposta, o sistema de IA forneceu a figura e as estratégias a seguir.

Estratégias:
• trace uma reta r que passe pelos pontos B e C;
• trace, no ponto C, uma reta s que seja perpendicular à reta r;
• denomine D o novo ponto em que a reta ; cruza a circunferência;
• ache o ponto médio do segmento 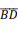 , que é o centro da circunferência, e o denomine E.
, que é o centro da circunferência, e o denomine E.
A circunferência representada por x2 + y2 - 6y - 7 está totalmente contida na circunferência criada pelo sistema de IA.