Questões do Enem Sobre química
Foram encontradas 472 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Para que se consiga atrair um maior número de abelhas para uma determinada região, a molécula que deve estar presente em alta concentração no produto a ser utilizado é:
Em um medicamento, a varfarina é administrada por via intravenosa na forma de solução aquosa, com concentração de 3,0 mg/mL. Um indivíduo adulto, com volume sanguíneo total de 5,0 L, será submetido a um tratamento com solução injetável desse medicamento.
Qual é o máximo volume da solução do medicamento que pode ser administrado a esse indivíduo, pela via intravenosa, de maneira que não ocorram hemorragias causadas pelo anticoagulante?
4 FeS2 (s) + 15O2 (g) + 2 H2O (I) ➙ 2 Fe2(SO4)3 (aq) + 2 H2 SO4 (aq)
FIGUEIREDO, B. R. Minérios e ambiente. Campinas: Unicamp, 2000.
Para corrigir os problemas ambientais causados por essa drenagem, a substância mais recomendada a ser adicionada ao meio é o
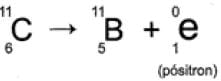
A partir da injeção de glicose marcada com esse nuclídeo, o tempo de aquisição de uma imagem de tomografia é de cinco meias-vidas.
Considerando que o medicamento contém 1,00 g do carbono-1 1 , a massa, em miligramas, do nuclídeo restante, após a aquisição da imagem, é mais próxima de
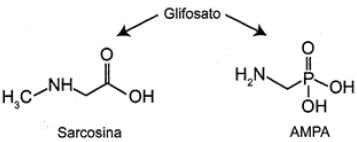
AMARANTE JR „ O. P. et al. Quimíca Nova. São Pauto, v. 25, n, 3, 2002 (adaptado).
A partir do texto e dos produtos de degradação apresentados, a estrutura química que representa o glifosato é: