Questões Militares de Química - Grandezas: massa, volume, mol, massa molar, constante de Avogadro e Estequiometria.
Foram encontradas 195 questões
No esboço da Tabela Periódica abaixo estão discriminados os números de nêutrons dos isótopos mais estáveis de alguns elementos.
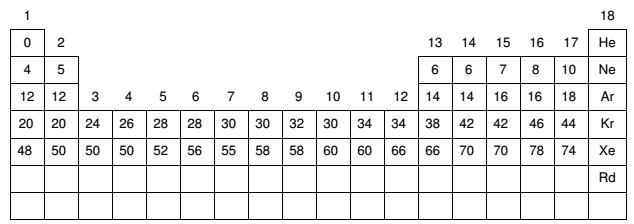
Considere agora um composto iônico binário, em que:
(i) o cátion, de carga +2, possui 12 prótons;
(ii) o ânion, de carga –3, possui 10 elétrons.
A massa de 1 mol deste composto é aproximadamente igual a:
Uma solução aquosa saturada de gás sulfídrico possui concentração igual a 0,1M e constante de ionização igual a 10-22 Calcule a concentração de sulfeto necessária para precipitação dos cátions do segundo Grupo, sabendo-se que o pH deve ser regulado para se obter uma solução 0,25M em ácido clorídrico, e assinale a opção correta.
Dados: H2S → 2 H+ + S-2
O fósforo elementar é, industrialmente, obtido pelo aquecimento do fosfato de cálcio com coque na presença de sílica de acordo com as seguintes reações:
2 Ca3 (PO4) 2 + 6 SiO2 → 6 CaSiO3 + P4O10
P4O10 + 10 C → P4 + 10 CO
Calcule quantos gramas de fosfato de cálcio são necessários
para produzir 46,5 g de fósforo elementar, e assinale a
opção correta.
O perclorato de potássio (KClO4) é usado como oxidante em propelentes e pirotécnicos. Calcule o calor necessário para aumentar a temperatura de 5,0 g de KClO4, de 25°C até 90° C, e assinale a opção correta.
Dado: Capacidade calorífica específica do KClO4 = 0,8111 J.K-1 . g-1