Questões Militares de Química
Foram encontradas 2.077 questões
Acerca dos diferentes tipos de ligações químicas e das substâncias formadas em reações químicas, julgue o próximo item.
Nas moléculas, os átomos das substâncias são organizados
linearmente de acordo com sua fórmula molecular.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
A massa molecular das substâncias é dada pela soma das
massas de todos os átomos que constituem suas moléculas
ou fórmulas mínimas.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
De acordo com o modelo atômico de Rutherford, os átomos
são constituídos de elétrons, prótons e nêutrons.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
Na tabela periódica, os elementos químicos são classificados
em subgrupos de elementos conforme as propriedades de seus
átomos.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
Os elementos químicos são organizados na tabela periódica
pelo crescente número de massa.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
Elemento químico pode ser considerado um conceito teórico,
por ser definido como tipo de átomos, também definido por
um número atômico.
A respeito da matéria e de sua constituição química, julgue o item a seguir.
O mol é a unidade de medida da grandeza quantidade
de matéria.
A respeito das propriedades químicas e físicas de determinados combustíveis, julgue o próximo item.
A gasolina é uma substância orgânica que reage com o
oxigênio do ar.
A respeito das propriedades químicas e físicas de determinados combustíveis, julgue o próximo item.
O etanol é uma substância inorgânica.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
A substância do extintor de pó químico é formada por ligações
covalentes e iônicas.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
No texto, são apresentadas fórmulas que contêm átomos de
elementos químicos de não metal e de um metal de transição.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
Quando em funcionamento, o extintor de espuma facilita o
contato do comburente com o combustível.
Com relação ao funcionamento desses tipos de extintores e aos seus componentes químicos, julgue o item a seguir.
A primeira substância citada no texto — NaHCO3 — pode ser
formada pela adição de CO2 a uma solução de hidróxido de
sódio.
Considere as duas moléculas abaixo:
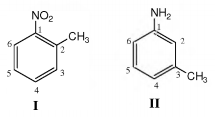
Ambas sofrerão nitração nos anéis aromáticos via substituição eletrofílica. Dentre as opções a seguir, a única
que indica posições passíveis de substituição nas moléculas I e II, respectivamente, é:
Considere as seguintes afirmativas:
I - Uma reação química a temperatura e pressão constantes será espontânea se a variação da energia livre de Gibbs (ΔG) for menor que zero.
II - Em um sistema reacional onde a única forma de trabalho observável é o trabalho de expansão, a variação da entalpia (ΔH) é igual à quantidade de calor liberada ou absorvida pela reação, a pressão constante.
III - Para uma substância simples que admite mais de uma forma alotrópica, não há variação de entalpia na conversão de uma forma em outra.
São corretas:
Dada a estrutura química da satratoxina-H abaixo, podemos afirmar que essa molécula possui:
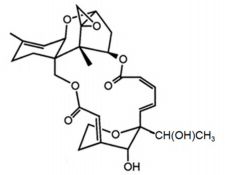
Considere o diagrama de fases simples para o benzeno, em que PC é o ponto crítico e PT o ponto triplo.
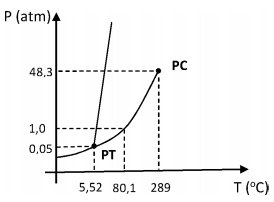
Os pontos de fusão e de ebulição do benzeno a 1,0 atm são iguais a 5,53 °C e 80,1 °C, respectivamente. Considere ainda, o ponto P (5,50 °C, 55 atm) como ponto de partida das transformações sequenciais discriminadas abaixo:
(1) Inicialmente, elevação da temperatura até 300 °C, em um processo isobárico;
(2) Redução da pressão até 38 atm, em um processo isotérmico;
(3) Redução da temperatura até 5,50 °C, em um processo isobárico;
(4) Finalmente, redução da pressão até 0,02 atm, em um processo isotérmico.
Assinale a alternativa que apresenta a ordem correta das mudanças de fase observadas ao longo do
processo descrito.
Dadas as seguintes equações que representam supostas reações químicas irreversíveis em meio aquoso e temperaturas moderadas:
I) 6 HBr + 2 Al → 2 AlBr3 + 3 H2
II) H2SO4 + BaCl2 → BaSO4 + 2 HCl
III) 2 KOH + NiSO4 → Ni(OH)2 + K2SO4
IV) 2 HBr + K2S → 2 KBr + H2S
V) BaCl2 + Na2CO3 → BaCO3 + 2 NaCl
Pode-se afirmar que a reação:
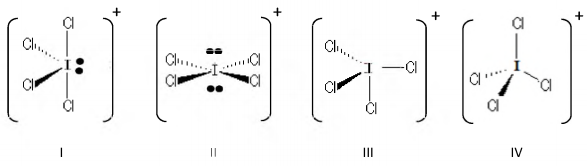
Assinale a alternativa que apresenta, respectivamente, a estrutura do íon ICl4+ e o tipo de hibridização de seu átomo central.