Questões Militares de Química - Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
Foram encontradas 101 questões
(Dados: log 1,49 = 0,17 e log 1,18 = 0,07.)
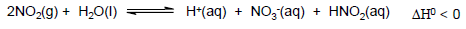
Num ensaio em laboratório, foram acondicionados num sistema fechado N2(g), O2(g), NO2(g) e vapor de água que está em equilíbrio com água líquida. A partir desses dados, considere as seguintes afirmações:
1. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema.
2. Um aquecimento brando tenderá a aumentar o pH da solução dentro do sistema.
3. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, diminuindo o pH da solução dentro do sistema.
4. A contribuição do ácido nitroso (HNO2) para o pH da solução dentro do sistema é desprezível.
Assinale a alternativa correta
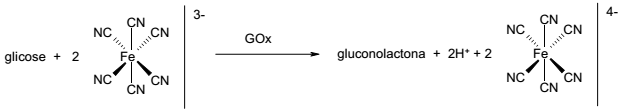
Nesse sistema de medição, faz-se reagir uma amostra contendo glicose com o íon ferricianeto ([Fe(CN)6]3- ) na presença da enzima GOx, obtendo-se como produtos gluconolactona, H+ e ferrocianeto ([Fe(CN)6]4- ). Um eletrodo de platina promove a reação de regeneração do ferricianeto, sendo que a corrente que passa por esse eletrodo é proporcional à concentração de glicose na amostra.
Com base no exposto, identifique como verdadeiras (V) ou falsas (F) as seguintes afirmativas:
( ) A enzima GOx catalisa a oxidação da glicose.
( ) No eletrodo de platina ocorre a redução do íon de ferro.
( ) A transformação de glicose em gluconolactona envolve 2 elétrons.
( ) O valor de pH do meio tende a diminuir no processo de detecção de glicose.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Marque a opção correta.
A dissociação do ácido acético em água ocorre de acordo com a seguinte equação:

Ao adicionar acetato de sódio ao sistema representado acima, supõe-se que o(s) efeito(s) observado(s) é(são):
I. pH diminui.
II. pH aumenta.
III. pKa diminui.
IV. pKa aumenta.
São feitas as seguintes comparações de valores de pKa de compostos orgânicos:
I. pKa (CH3COOH) > pKa (CℓCH2COOH)
II. pKa (F3CCOOH) > pKa (Cℓ3CCOOH)
III. pKa (CH3CH2CHCℓCOOH) > pKa (CH3CHCℓCH2COOH)
Das comparações acima, está(ão) CORRETA(S) apenas