Questões Militares
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 291 questões
Bebidas especialmente ingeridas por esportistas têm representado importante fatia de consumo. Tais bebidas são soluções isotônicas repositoras hidroeletrolíticas e, portanto, auxiliam na manutenção e preparação física de atletas de todas as modalidades. A seguir, reproduz-se parte da tabela nutricional constante no rótulo de uma dessas bebidas.

A partir dessas informações e considerando os múltiplos aspectos que
elas suscitam, julgue o item subsequente.
Na referida bebida, a concentração de íons cloreto é inferior a
0,010 mol/L.
Bebidas especialmente ingeridas por esportistas têm representado importante fatia de consumo. Tais bebidas são soluções isotônicas repositoras hidroeletrolíticas e, portanto, auxiliam na manutenção e preparação física de atletas de todas as modalidades. A seguir, reproduz-se parte da tabela nutricional constante no rótulo de uma dessas bebidas.

A partir dessas informações e considerando os múltiplos aspectos que
elas suscitam, julgue o item subsequente.
Considerando-se o valor aproximado de 6×1023 mol-1 para a
constante de Avogadro, conclui-se que é superior a 3×1020 a
quantidade de íons potássio presente em 1 copo de 200 mL da
referida bebida isotônica.
Uma solução aquosa saturada de gás sulfídrico possui concentração igual a 0,1M e constante de ionização igual a 10-22 Calcule a concentração de sulfeto necessária para precipitação dos cátions do segundo Grupo, sabendo-se que o pH deve ser regulado para se obter uma solução 0,25M em ácido clorídrico, e assinale a opção correta.
Dados: H2S → 2 H+ + S-2
Analise as equações a seguir.
I - HF + H2O → H3O+ + F-
II - HCl + NH3 → NH4+ + Cl-
III- HNO3 + H2O → H3O+ + NO3-
De acordo com o conceito de ácido-base de Bronsted-Lowry, é INCORRETO afirmar que na equação
Considere uma amostra aquosa em equilíbrio a 60 °C, com pH de 6,5, a respeito da qual são feitas as seguintes afirmações:
I. A amostra pode ser composta de água pura.
II. A concentração molar de H3O+ é igual à concentração de OH − .
III. O pH da amostra não varia com a temperatura.
IV. A constante de ionização da amostra depende da temperatura.
V. A amostra pode ser uma solução aquosa 0,1mol.L−1em H2 CO3, considerando que a constante de dissociação do H2 CO3 é da ordem de 1 x 10−7 .
Das afirmações acima está(ão) CORRETA(S) apenas
Considere as seguintes afirmações a respeito dos haletos de hidrogênio HF HCl HBr e HI :
I. A temperatura de ebulição do HI é maior do que a dos demais. I
I. À exceção do HF ,os haletos de hidrogênio dissociam-se completamente em água.
III. Quando dissolvidos em ácido acético glacial puro, todos se comportam como ácidos, conforme a seguinte ordem de força ácida: HI > HBr > HCl >> HF
Das afirmações acima, está(ão) CORRETA(S) apenas
Considere as seguintes misturas (soluto/solvente) na concentração de 10 % em mol de soluto:
I. acetona/clorofórmio
II. água/etanol
III. água/metanol
IV. benzeno/tolueno
V. n-hexano/n-heptano
Assinale a opção que apresenta a(s) mistura(s) para a(s) qual(is) a pressão de vapor do solvente na mistura é
aproximadamente igual à sua pressão de vapor quando puro multiplicada pela sua respectiva fração molar.
Hidrogênio - 1 Carbono - 12 Nitrogênio - 14 Oxigênio - 16 Sódio - 23 Enxofre - 32 Cloro - 35,5 Cálcio - 40
Espera-se que uma fração menor das moléculas de H2SO4 sofra a segunda ionização após o tratamento da água contaminada do lago com um composto químico básico.
O óxido de cálcio (CaO) é um óxido ácido.
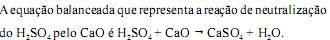
Assinale a opção que apresenta, respectivamente, o tipo de ligações que são encontradas na molécula representada pela fórmula N204 e o nome deste composto.
Um antiácido estomacal contém bicarbonato de sódio (NaHCO3) que neutraliza o excesso de ácido clorídrico (HCl), no suco gástrico, aliviando os sintomas da azia, segundo a equação:
HCl(aq) + NaHCO3(aq) → NaCl(aq) + H2O(l) + CO2(g)
Sobre essas substâncias, são feitas as seguintes afirmações:
I-A fórmula estrutural do bicarbonato de sódio e do ácido clorídrico são respectivamente:
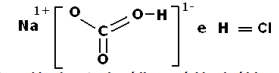
II-Na reação entre o bicarbonato de sódio e o ácido clorídrico, ocorre uma reação de oxidorredução.
III-O antiácido contém 4,200 g de bicarbonato de sódio para neutralização total de 1,825 g do ácido clorídrico presente no suco gástrico.
Dados:
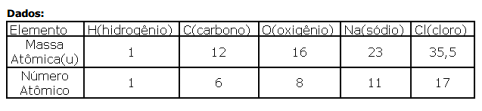
Das afirmações feitas, está(ão) correta(s)
A composição química do cimento Portland, utilizado na construção civil, varia ligeiramente conforme o que está indicado na tabela abaixo:
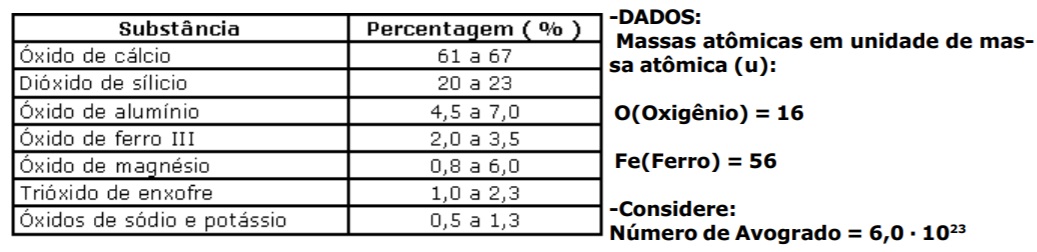
Assinale a alternativa correta: