Questões Militares
Sobre soluções e substâncias inorgânicas em química
Foram encontradas 286 questões
É provável que muitos alunos conheçam a clássica questão: “o que pesa mais, um quilo de chumbo ou um quilo de algodão?” Na verdade, eles têm a mesma massa, porém, os volumes que ocupam é que são diferentes.
A propriedade dessas matérias em que o
chumbo tem a sua massa contida em um
pequeno volume, enquanto o algodão tem sua
massa ocupando um grande volume, é definida
pela(o):
A água pura, o ácido clorídrico puro (HCl) e o ácido acético puro (CH3COOH) são maus condutores de corrente elétrica. Porém, esses ácidos em solução aquosa são condutores de eletricidade.
Uma solução aquosa diluída de HCl conduz a
corrente elétrica melhor que a de ácido acético
em solução porque:
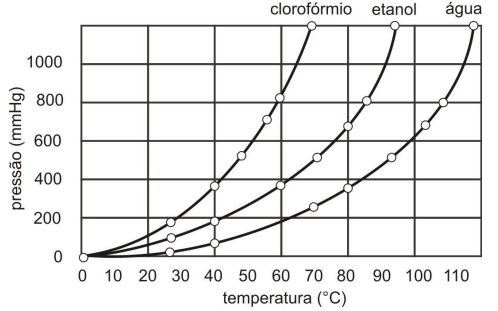
De acordo com o gráfico, é CORRETO afirmar que
Solução do frasco I: ficou rosa em fenolftaleína e amarela no metilorange.
Solução do frasco II: permaneceu incolor em fenolftaleína e vermelha no metilorange.
Solução do frasco III: permaneceu incolor em fenolftaleína e amarela no metilorange.
Sabe-se que a fenolftaleína, em pH acima de 9 apresenta coloração vermelha, enquanto que, em pH abaixo desse valor, é incolor. Sabe-se ainda que o metilorange apresenta coloração vermelha em pH abaixo de 3,5 e amarela em pH acima deste valor.
Sendo assim, os estudantes chegaram à conclusão de que os frascos I, II e III contêm, respectivamente, solução de
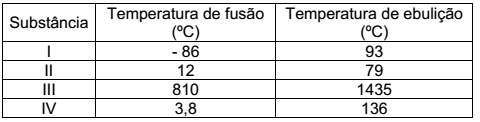
Em relação ao estado físico dessas substâncias, é CORRETO afirmar que
Considere as seguintes afirmações:
I. Um coloide é formado por uma fase dispersa e outra dispersante, ambas no estado gasoso.
II. As ligações químicas em cerâmicas podem ser do tipo covalente ou iônica.
III. Cristal líquido apresenta uma ou mais fases organizadas acima do ponto de fusão do sólido correspondente.
Então, das afirmações acima, está(ão) CORRETA(S)
A 25 °C, as massas específicas do etanol e da água, ambos puros, são 0,8 g cm−3 e 1,0 g cm−3 , respectivamente. Adicionando 72 g de água pura a 928 g de etanol puro, obteve-se uma solução com 1208 cm3 de volume.
Assinale a opção que expressa a concentração desta solução em graus Gay-Lussac (°GL).
A 25 °C, três frascos (I, II e III) contêm, respectivamente, soluções aquosas 0,10 mol L−1 em acetato de sódio, em cloreto de sódio e em nitrito de sódio.
Assinale a opção que apresenta a ordem crescente CORRETA de valores de pHx (x = I,II e III) dessas soluções, sabendo que as constantes de dissociação (K) , a 25 °C, dos ácidos clorídrico (HCl) , nitroso (HNO2) e acético (CH3COOH) , apresentam a seguinte relação:
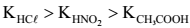
( ) Espécies químicas que têm na sua composição hidrogênio com carga parcial positiva, Hδ+, são ácidos de Arrhenius.
( ) Bases de Brönsted-Lowry têm na sua composição átomos com pares de elétrons não-ligantes.
( ) Bases de Brönsted-Lowry, em água, produzem íons OH-.
( ) Ácidos de Arrhenius são substâncias iônicas.
I. Ambas as etapas 1 e 2 ocorrem com absorção de calor.
II. Se a energia da etapa 3 suplantar a soma de 1 e 2, o processo é exotérmico.
III. A etapa 3 pode ser exotérmica ou endotérmica a depender do soluto.
IV. Se a soma de 1 e 2 for maior que o módulo de 3, a dissolução libera calor.
V. Se a energia para separar as partículas do soluto for elevada, não ocorrerá a dissolução.
