Questões Militares
Sobre transformações químicas em química
Foram encontradas 475 questões
14 KMnO4 + 4 C3 H5 (OH)3 → 7 K2 CO3 + 7 Mn2 O3 + 5 CO2 + 16 H2 O
O agente oxidante e a variação do número de oxidação do elemento manganês nessa reação são, respectivamente,
( ) Matéria é algo que possui massa e ocupa lugar no espaço. ( ) Toda matéria é classificada, exclusivamente, como elemento. ( ) Os átomos são constituídos, exclusivamente, pelas seguintes partículas subatômicas: elétrons e nêutrons. ( ) O próton é a carga positiva (+) fundamental da eletricidade e ele gira em torno do núcleo em trajetórias de “camadas” concêntricas.
I. CH4 (g) + O2 (g) → CO2 (g) + H2O (g)
II. CaO (s) + CO2 (g) → CaCO3 (s)
III. PbCO3 (s) → PbO (s) + CO2 (g)
IV. 2N2 (g) + 3H2 (g) → 2NH3 (g)
V. Fe (s) + 2HCl (aq) → FeCl2 (aq) + H2 (g)
Assinale a alternativa que classifica corretamente a reação apresentada.
Adaptado. Disponível em: Cobre: Ocorrência, obtenção industrial, propriedades e utilização - UOL Educação. Acesso: 05 de janeiro de 2022.
Um dos minérios mais utilizados na obtenção do cobre metálico é a calcosita, que pode ser representada pela fórmula Cu2 S. Um método de retirada do enxofre do minério é o processo de ustulação (por meio de aquecimento em presença de ar seco, rico em gás oxigênio). Observe a equação não balanceada a seguir, que representa o processo citado anteriormente:
Cu2S + O2 → Cu + SO2
Após o balanceamento da equação anterior, assinale a alternativa que apresenta qual é a massa aproximada (em gramas) de cobre metálico que pode ser obtida a partir de 2,0 Kg de Cu2S, com 60% de pureza e gás oxigênio suficiente. (Dados: massas atômicas - Cu = 63,5; S = 32).
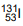 radioativo foi empregado pela primeira vez em 1941 no Massachusetts General Hospital, quando Hertz e Roberts trataram pacientes com hipertireoidismo. Dependendo da dose de iodo radioativo administrada, pode ser necessária a internação do
paciente, geralmente em um quarto especial para impedir que outras pessoas sejam expostas à radiação. O isótopo
radioativo foi empregado pela primeira vez em 1941 no Massachusetts General Hospital, quando Hertz e Roberts trataram pacientes com hipertireoidismo. Dependendo da dose de iodo radioativo administrada, pode ser necessária a internação do
paciente, geralmente em um quarto especial para impedir que outras pessoas sejam expostas à radiação. O isótopo 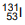 possui
possui O elemento químico mais eletronegativo, localizado no grupo 17 e no segundo período da Tabela Periódica, tende a formar I de carga II para ficar mais estável e, nessa configuração, sua última camada eletrônica possui III elétrons.
Esse elemento se associa ao hidrogênio, formando uma substância que pode ser usada para criar situações de destruição em massa, uma vez que produz efeitos sistêmicos decorrentes da hipocalcemia, hipomagnesemia e hiperpotassemia, além da possível ocorrência de coagulopatia e arritmias cardíacas fatais. (Disponível em: https://www.msdmanuals.com/pt-br. Adaptado)
Completam, correta e respectivamente, as lacunas I, II e III:
Massa molar: O=16 g/mol; H=1 g/mol; C=12 g/mol.
Número atômico dos elementos: O=8; F=9; Na=11.