Questões Militares
Sobre velocidade de reação, energia de ativação, concentração, pressão, temperatura e catalisador em química
Foram encontradas 77 questões
Analise o diagrama a seguir.

O diagrama está representando uma reação
I. Amaciamento de carne pela adição de papaína. II. Conservação de frutas em geladeira. III. Antiácido efervescente em pó colocado na água.
Os fatores que alteram a rapidez das reações nas situações I, II e III são, respectivamente,
Considere a reação a seguir:
2 NO + 2 H2 → N2 + 2 H2 O
A lei da velocidade para a reação é de segunda ordem
para o NO e de primeira ordem para o H2
. Portanto, ao
dobrar a concentração de NO mantendo-se a concentração de H2
, a velocidade da reação é:
Na + CH3 CH2 OH → CH3 CH2 ONa + H2
Considerando que nas CATP (Condições Ambientais de Temperatura e Pressão) 1 mol de qualquer gás ocupa 25 L, o volume de H2 produzido, quando reagem 1 g de sódio e 1 g etanol, e a massa do excesso de reagente são, respectivamente,
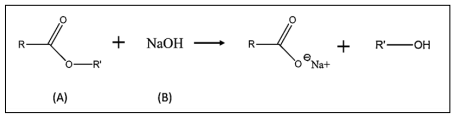
Considere que a reação simbolizada foi estudada no quesito cinético. Os dados empíricos das velocidades iniciais medidas para diferentes concentrações iniciais dos reagentes são mostrados no quadro:
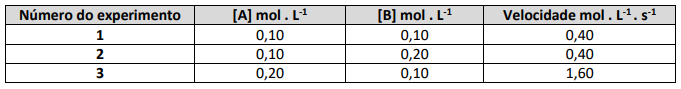
Com base nas informações fornecidas, a velocidade da reação (em mol . L-1 . s-1 ), quando [A] = 0,30 mol . L-1 e [B] for 0,10 mol . L-1 , será de:
Os dados do estudo cinético de uma reação representada por
2 A → 2B + 3C
possibilitaram construção de uma curva de rapidez da reação, representada na figura a seguir.
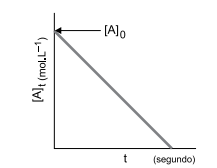
(P. Atkins; L. Jones; Princípios de Química: questionando a vida
moderna e o meio ambiente. 5a
ed. Trad. Ricardo Bicca de Alencastro.
Porto Alegre: Bookman, 2012. Adaptado)
A ordem dessa reação e as unidades de sua constante
de velocidade são:
1. Há consumo de CYP3A4 no decorrer da reação.
2. A losartana e o CYP3A4 são reagentes da reação.
3. O CYP3A4 diminui a energia de ativação da reação.
4. O estado de equilíbrio da reação é alterado pelo CYP3A4 no sentido de formar mais derivado carboxilado.
Assinale a alternativa correta.
Considere a equação da reação hipotética: X + Y + Z → W + T + Q
São conhecidos os seguintes resultados do estudo cinético desta reação, obtidos nas mesmas condições experimentais:
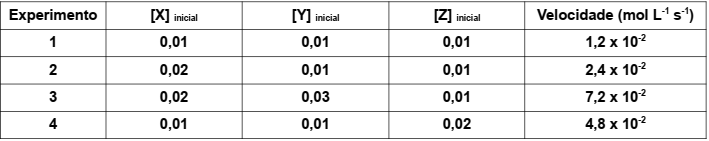
Considere [ ] = concentração mol L-1
.
A partir das observações experimentais, conclui-se que a equação da velocidade para a reação é
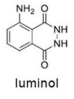
Tendo como referência a estrutura do luminol, apresentada anteriormente, e as informações do texto precedente, julgue o item a seguir, considerando que MH = 1 g/mol, MC = 12 g/mol, MN = 14 g/mol e MO = 16 g/mol.
O ferro presente na hemoglobina atua como catalisador na
reação do luminol com o sangue.
Constantes
Constante de Avogadro (NA) = 6,02 × 1023 mol−1
Constante de Faraday (F) = 9,65 × 104 C⋅mol−1 = 9,65 × 104 A⋅s⋅mol−1 = 9,65 × 104 J⋅V−1 ⋅mol−1
Carga elementar = 1,60 × 10−19 C
Constante dos gases (R) = 8,21 × 10−2 atm⋅L⋅K−1⋅mol−1 = 8,31 J⋅K −1 ⋅mol−1 = 1,98 cal⋅K−1 ⋅mol−1
Constante de Planck (h) = 6,63 × 10−34 J⋅s
Velocidade da luz no vácuo = 3,0 × 108 m⋅s −1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 × 105 N⋅m−2 = 1,01325 bar
Energia: 1 J = 1 N⋅m = 1 kg⋅m2 ⋅s−2 = 6,24 × 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 °C e 1 atm
Condições ambientes: 25 °C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol⋅L−1 (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol⋅L−1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio

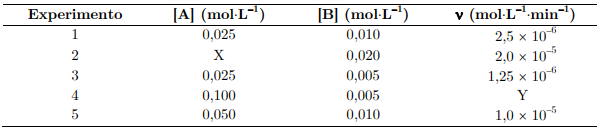
Com base nesses experimentos, assinale a opção que apresenta os valores corretos de α, β, k, X e Y, respectivamente.
Analise o diagrama.
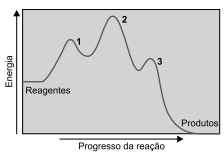
O diagrama representa uma reação _________, que ocorre em três etapas, sendo a mais _________ a etapa 3, porque possui _________ energia de ativação.
Assinale a alternativa que completa, correta e respectivamente, as lacunas.
Analise o diagrama.
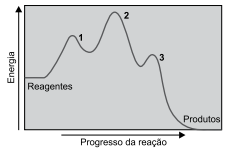
O diagrama representa uma reação _______________ , que ocorre em três etapas, sendo a mais ____________ a etapa 3, porque possui ____________ energia de ativação.
Assinale a alternativa que completa, correta e respectivamente, as lacunas.
É requerido que fazendas produtoras de leite bovino controlem a acidez do leite que está aguardando o processamento. Essa acidez é resultante da conversão da lactose em ácido lático (ácido 2-hidroxipropanoico) por ação de microrganismos:
C12H22O11 + H2O → 4C3H6O3
Um fazendeiro decidiu fazer um experimento para determinar a taxa de geração de ácido lático no leite armazenado: retirou uma amostra de 50 cm3 de leite, cuja concentração de ácido lático é de 1,8 g/L, e, depois de três horas, utilizou 40 cm3 de uma solução 0,1 molar de NaOH para neutralizá-la.
Conclui-se que a taxa média de produção de ácido lático por litro de leite é:
Uma amostra de gás metano, CH4, foi aquecida lentamente na pressão constante de 0,90 bar. O volume do gás foi medido em diferentes temperaturas e um gráfico de volume versus temperatura foi construído. Sabendo que inclinação da reta foi 2,88x10-4 L/K, calcule a massa do gás metano e assinale a opção correta.
Dados:
R = 0,082 atm L mol-1 K-1
1 bar = 1 atm
As seguintes velocidades iniciais foram obtidas como dados experimentais para uma reação hipotética 2A + B → C + 3D:

Considerando os dados acima, qual é a equação de
velocidade da reação e o valor da constante de
velocidade, respectivamente?
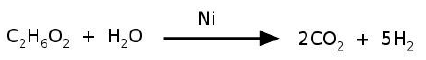
Nas condições mencionadas, a reação de reforma ocorre num tempo menor quando usado o níquel poroso porque:
