Questões de Concurso Militar ITA 2016 para Aluno - Química
Foram encontradas 17 questões
CONSTANTES

DEFINIÇÕES


I. Alumínio II. Magnésio III. Paládio IV. Sódio V. Zinco
Assinale a opção que apresenta o(s) metal(is) de sacrifício que pode(m) ser utilizado(s).
CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


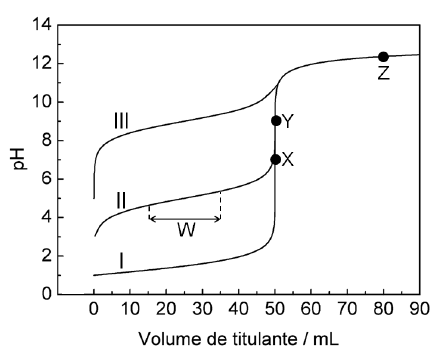
Na figura ao lado são respectivamente apresentadas as curvas de titulação de 50 mL de soluções aquosas 0,1 mol·L-1 dos ácidos I, II e III, tituladas com uma solução aquosa 0,1 mol·L-1 em NaOH. Baseado nas informações contidas na figura, assinale opção ERRADA.
CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


I. Etanoato de etila com amônia forma etanamida e etanol. II. Ácido etanóico com tricloreto de fósforo, a quente, forma cloreto de etanoíla. III. n-Butilbenzeno com permanganato de potássio, a quente, forma ácido benzóico e dióxido de carbono.
Das proposições acima, está(ão) CORRETA(S)
CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


Considere as seguintes proposições para espécies químicas no estado gasoso:
I. A energia de ionização do íon Be3+ é maior do que a do íon He+ .
II. O momento dipolar elétrico total da molécula de XeF4 é maior do que o da molécula de XeF2.
III. A energia necessária para quebrar a molécula de F2 é maior do que a energia necessária para quebrar a molécula de O2.
IV. A energia do orbital 2s do átomo de berílio é igual à energia do orbital 2s do átomo de boro.
Das proposições acima, está(ão) CORRETA(S)
CONSTANTES

DEFINIÇÕES


Considere as proposições a seguir:
I. A reação do ácido butanóico com a metilamina forma N-metil-butanamida.
II. A reação do ácido propanóico com 1-propanol forma propanoato de propila.
III. 3-etil-2,2-dimetil-pentano é um isômero estrutural do 2,2,3,4-tetrametil-pentano.
IV. O 2-propanol é um composto quiral.
Das proposições acima estão CORRETAS
CONSTANTES

DEFINIÇÕES


CONSTANTES

DEFINIÇÕES


São feitas as seguintes proposições a respeito dos hidrocarbonetos cuja fórmula molecular é C5H10:
I. Existem apenas seis isômeros do C5H10.
II. Pelo menos um dos isômeros do C5H10 é quiral.
III. Em condições ambiente e na ausência de luz todos os isômeros do C5H10 são capazes de descolorir água de bromo.
Das proposições acima é (são) CORRETA(S)